Для чего нужны белки в клетке: Зачем нам нужны белки и как их правильно употреблять. Блог фитнес-тренера / НВ
Белок в организме: функции, норма, продукты, признаки дефицита :: Здоровье :: РБК Стиль
Материал проверила и прокомментировала Горбачёва Наталья Леонидовна, диабетолог, диетолог, эндокринолог, ведущий специалист сети клиник «Семейная»
Что такое белок
Белки — главный строительный материал организма. Он участвует в создании мышц, сухожилий, органов и кожи, а также нужен для производства ферментов, гормонов, нейромедиаторов и различных молекул, которые выполняют множество важных функций. Белки состоят из более мелких молекул, аминокислот, которые соединяются вместе, как бусы на нитке. Эти связанные аминокислоты образуют длинные белковые цепи, которые затем складываются в сложные формы. Некоторые аминокислоты организм производит самостоятельно, другие можно восполнить только с помощью еды.
Функции белка в организме
Рост мышц и повышение выносливости
Организму необходим протеин, ведь мышцы в основном состоят из белка.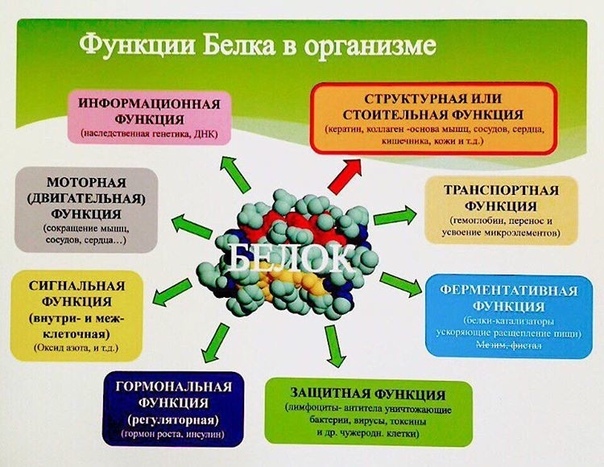
Биохимические процессы
Белки — ферменты, они помогают тысячам биохимических реакций, происходящих внутри клеток организма [3]. В том числе активируют метаболизм посредством объединения с другими молекулами — субстратами. Ферменты также могут функционировать и вне клетки, например, пищеварительные — лактоза и сахароза, которые помогают переваривать сахар. От их количества зависит пищеварение, свертывание крови и энергетический баланс. Дисбаланс некоторых ферментов может привести к сбоям в работе большинства систем организма [4].
Гормональный баланс
Некоторые белки представляют собой гормоны, которые как химические посредники помогают взаимодействовать различным клеткам организма. Их производят эндокринные ткани и железы, а затем белки транспортируются по внутренним органам. Эти гормоны делят на три группы: белок и пептиды, стероиды и амины [5].
Структура тканей
Некоторые белки являются волокнами, придающими жесткость клеткам: кератин, коллаген и эластин. Они помогают формировать каркас тканей тела [6]. Кератин — строительный материал для кожи, волос и ногтей, коллаген — структурный белок костей, кожи, связок и сухожилий, а эластин позволяет тканям возвращаться в первоначальную форму после растяжений и сокращений.
Правильный pH
Белок играет жизненно важную роль в регулировании концентрации кислот и оснований в крови и других жидкостях организма [7].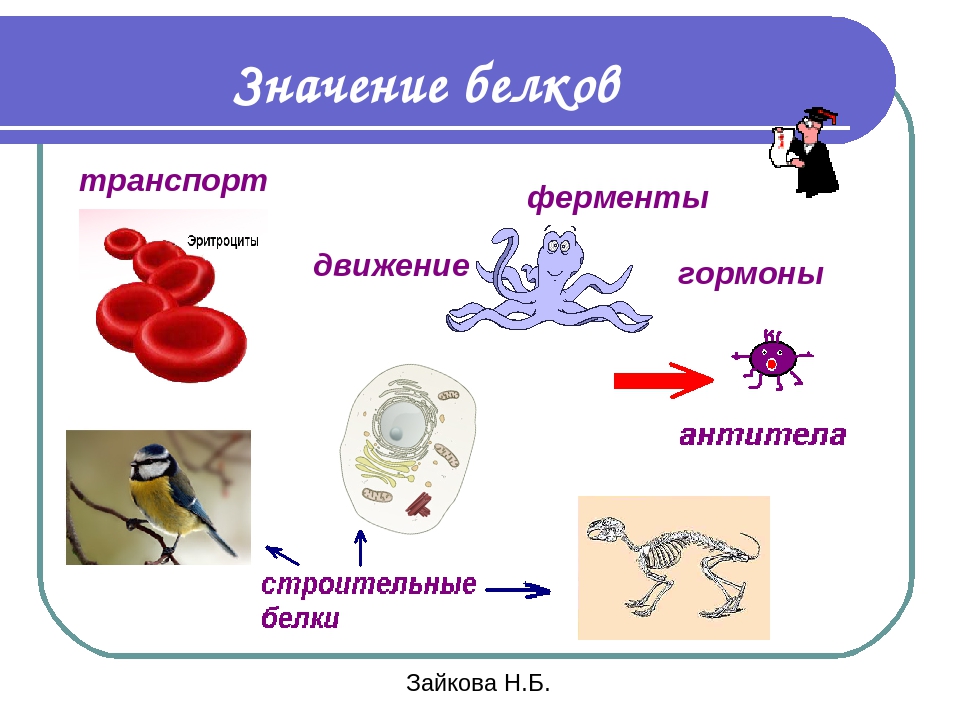 Этот баланс измеряется с помощью шкалы pH от 0 до 14, где 0 — максимально кислый, 7 — нейтральный, 14 — наиболее щелочной. Протеины — один из способов регулирования этих показателей. Например, гемоглобин — тоже белок, из которого состоят эритроциты. Он связывает небольшое количество кислоты, помогая поддерживать нормальный уровень pH в крови.
Этот баланс измеряется с помощью шкалы pH от 0 до 14, где 0 — максимально кислый, 7 — нейтральный, 14 — наиболее щелочной. Протеины — один из способов регулирования этих показателей. Например, гемоглобин — тоже белок, из которого состоят эритроциты. Он связывает небольшое количество кислоты, помогая поддерживать нормальный уровень pH в крови.
Хороший иммунитет
Белки помогают формировать иммуноглобулины или антитела для борьбы с инфекцией [8] [9]. Антитела — белки в крови, которые помогают защитить организм от бактерий и вирусов. Вырабатывая их в качестве реакции на вторжение чужеродных элементов, клетки в дальнейшем лучше противостоят похожим заболеваниям.
Баланс жидкости
Альбумин и глобулин — белки крови, которые помогают сохранить баланс жидкости в организме, удерживая воду в клетках [10] [11]. При недостатке протеина могут возникать отеки, так как жидкость вытесняется в промежутки между клетками [12].
Нормализация веса
Белок важен для тех, кому необходимо нормализовать вес. Некоторые эксперименты ученых подтверждают, что увеличение количества белка в рационе ведет к повышению скорости метаболизма и снижению аппетита [13]. Протеин хорошо насыщает, в результате чего реже хочется перекусывать, снижается объем порций в основных приемах пищи [14] [15]. В одном из исследований женщины 12 недель употребляли белковую пищу в количестве 30% от дневной калорийности рациона. В среднем каждая из участниц эксперимента потеряла порядка пяти килограмм веса, сохранив здоровые пищевые привычки [16].
Некоторые эксперименты ученых подтверждают, что увеличение количества белка в рационе ведет к повышению скорости метаболизма и снижению аппетита [13]. Протеин хорошо насыщает, в результате чего реже хочется перекусывать, снижается объем порций в основных приемах пищи [14] [15]. В одном из исследований женщины 12 недель употребляли белковую пищу в количестве 30% от дневной калорийности рациона. В среднем каждая из участниц эксперимента потеряла порядка пяти килограмм веса, сохранив здоровые пищевые привычки [16].
Норма белка в день
Если вы каждый день едите продукты животного происхождения, такие как мясо, рыбу, яйца или молочные продукты, вы, вероятно, получаете достаточно белка. Если придерживаетесь растительной диеты, получить незаменимые аминокислоты, необходимые организму, будет сложнее. Среднестатистические нормы протеина в рационе на один килограмм веса:
- для женщин – 60–90 г;
- для мужчин – 80–150 г;
- для дошкольников – 3 г;
- для школьников – 2,5 г.

В некоторых случаях требуется больше белка, например, в периоды болезни, интенсивных занятий спортом, а также при беременности и кормлении грудью [17] [18]. Данные о точном количестве вещества разнятся, поэтому правильно будет проконсультироваться с лечащим врачом, который подберет индивидуальный рацион, исходя из особенностей организма. Так, авторы одного исследования утверждают, что беременным женщинам в день необходимы 1,2–1,52 г протеина на один кг веса [19]. Другие врачи рекомендуют потреблять дополнительно 1,1г белка на кг веса [20]. Суточная норма белка во время грудного вскармливания составляет 1,3 г на килограмм в день плюс 25 дополнительных граммов [21].
Активным людям требуется больше белка, чем тем, кто ведет малоподвижный образ жизни. Спортсменам, предпочитающим тренировки на выносливость, необходимо около 1,2–1,4 г на каждый кг веса [22] [23]. Достаточное количество протеина необходимо для предотвращения развития заболеваний, таких как остеопороз. Пожилым людям, а также тем, кто восстанавливается после травмы или операции, требуется до 1–1,3 г на один кг массы тела [24] [25].
Пожилым людям, а также тем, кто восстанавливается после травмы или операции, требуется до 1–1,3 г на один кг массы тела [24] [25].
Сколько белка в яйцах, курице и твороге
-
Яйца. Содержат 6-7 г белка на штуку среднего размера. Содержатся они именно в белковой части яйца. Поэтому в фитнес-меню часто присутствуют блюда без желтка, но на самом деле, при сбалансированном рационе нет смысла от них отказываться.
-
Курица. Если необходимо добавить белка в рацион, выбирайте куриную грудку — в ней больше волокон и меньше жира. На 100 г продукта — 27% белка. Оптимальный ингредиент для повышения уровня белка в организме, если вы не придерживаетесь растительной диеты.

-
Творог. В 200-граммовой пачке творога содержится 35 г белка, что соответствует почти трети среднестатистической дневной нормы. Отдавайте предпочтение творогу средней жирности, так как обезжиренного усваивается меньше необходимым микроэлементов.
Продукты, богатые белком
В первую очередь, протеин попадает в организм из животных продуктов. Средние показатели белка на 100 г продукта:
- птица — 27 г;
- свинина — 27 г;
- говядина — 26 г;
- рыба — 22 г;
- морепродукты — 22 г.
Вегетарианцам и веганам стоит позаботиться о наличии растительного белка в рационе. Это могут быть бобовые, крупы, соевые и цельнозерновые продукты:
- красная чечевица — 18 г белка;
- красная фасоль — 16 г;
- маш, нут, черная фасоль — 14 г;
- гречка и цельнозерновой хлеб — 13 г;
- киноа и тофу — 8 г;
- тыквенные семечки — 5 г в одной порции (горсть 25-30 г).

Норма белка в моче и крови
Лучший способ проверить, хватает ли организму белка, — сдать анализы, например биохимический анализ крови. В норме концентрация белка в крови взрослого человека должна составлять 62–86 г/л, а у детей — от 45 до 80 г/л. Снижение этих показателей возникает в результате ряда заболеваний, в том числе первичных иммунодефицитов, нарушениях обмена веществ, дисфункциях желудочно-кишечного тракта, а также дефицита протеина в рационе.
Превышение нормы встречается редко, но оно может указывать на хронические тяжелые инфекции (такие как туберкулез), ускоренный распад эритроцитов, системные опухоли или обезвоживание организма.
С-реактивный белок — фракция протеинов плазмы, которая повышается при наличии в организме воспалительного процесса. Синтезируется в ответ на попадание в кровь токсинов патологических микроорганизмов и обезвреживает их путем их связывания, а также запускает иммунные реакции.
Помимо крови, белок учитывают в анализе мочи. Небольшое его количество встречается и у здоровых людей, в норме — до 140 мг/л (до 0,140 г/л). При активной физической нагрузке показатели не должны превышать 250 мг/сутки (0,250 г/л). Для того, что точнее узнать потери белка с мочой, необходимо проводить исследование его концентрации в суточных анализах. Их назначают при заболеваниях мочевыделительной системы и почек, инфекциях, а также для контроля осложнений, в том числе при приеме препаратов, оказывающих нефротоксическое действие — поражение почек.
Переизбыток белка
Высокое потребление белка может нанести вред людям с заболеваниями почек [26]. Двумя основными факторами риска почечной недостаточности являются высокое кровяное давление (гипертония) и диабет. И то, и другое провоцируется переизбытком белка [27] [28]. Точное количество необходимого протеина варьируется в зависимости от возраста, состояния здоровья и образа жизни. Исследование с участием здоровых мужчин, занимающихся силовыми тренировками, показало, что ежедневное употребление 3 г белка на кг массы тела в течение года не имело никаких неблагоприятных последствий для здоровья [29]. Даже 4,4 г на кг веса в течение двух месяцев не вызывало никаких побочных эффектов [30].
И то, и другое провоцируется переизбытком белка [27] [28]. Точное количество необходимого протеина варьируется в зависимости от возраста, состояния здоровья и образа жизни. Исследование с участием здоровых мужчин, занимающихся силовыми тренировками, показало, что ежедневное употребление 3 г белка на кг массы тела в течение года не имело никаких неблагоприятных последствий для здоровья [29]. Даже 4,4 г на кг веса в течение двух месяцев не вызывало никаких побочных эффектов [30].
Нет никаких доказательств того, что потребление белка в разумных количествах причиняет вред здоровым людям. Напротив, существует множество доказанных преимуществ. Однако, если у вас заболевание почек, следует следовать советам врача и ограничить потребление протеинов.
Богатое белками, но бедное жирами и углеводами питание — нагрузка на почки и печень. Переизбыток белка на фоне нехватки других необходимых организму веществ выражается в проблемах с пищеварением, неприятном запахе изо рта и постоянной жажде.
Недостаток белка
Помимо показателей медицинских анализов есть и другие признаки недостатка протеина, которые вы можете заметить перед походом к врачу.
Постоянный голод
Белки насыщают и заряжают энергией надолго, но в качестве перекуса многие из нас используют не белковые продукты, а содержащие углеводы: бананы, печенье, конфеты, выпечку и бутерброды. Еда, богатая углеводами, приводит к быстрому подъему уровня сахара (и мы чувствуем себя сытыми) и такому же быстрому падению (через полчаса мы снова голодны). Этот же эффект вызывает тягу к сладкому: организму не хватает сил, а конфета — самый быстрый способ их получить. Правда, ненадолго.
Слабые волосы и ногти
Ногти и волосы — это тоже белок, а точнее, кератин. Для их здоровья регулярное потребление белковой пищи абсолютно необходимо, иначе организму неоткуда будет брать строительный материал. При дефиците белка волосы становятся тонкими, слабыми и тусклыми, плохо растут и секутся, а ногти начинают ломаться и расслаиваться.
Медленное заживление ран
Если даже маленькая царапина заживает дольше недели, это тоже может быть признаком недостатка белка. Он входит в состав клеток мышечной ткани, кожи и крови, поэтому, если макроэлемента не хватает, на ремонт повреждений у организма уходит гораздо больше времени.
Частые инфекционные болезни
По мнению доктора Алиссы Рамси из американской Академии питания и диетологии, белок также необходим для построения клеток иммунной системы — если вы едите мало белковых продуктов, со временем защита организма может ослабеть.
Без белка замедляется выработка интерферона и лизоцима, «защитников», отбивающих атаки патогенов. Иммунитет перестает справляться с бактериями и вирусами, и мы болеем чаще. Причем любыми инфекционными заболеваниями: у людей на низкобелковой диете часто диагностируют инфекции.
Отеки
Дефицит белка приводит к нарушению водно-солевого баланса, из-за чего жидкость скапливается в тканях. Результат — мешки под глазами и опухшее по утрам лицо, отеки лодыжек и стоп, чувство тяжести в ногах, которое появляется уже в середине дня, даже если вы носите удобную обувь.
Результат — мешки под глазами и опухшее по утрам лицо, отеки лодыжек и стоп, чувство тяжести в ногах, которое появляется уже в середине дня, даже если вы носите удобную обувь.
Снижение веса
У нашего организма свои приоритеты. Если белка не хватает, то все поступающие протеины направляются туда, где они жизненно необходимы, то есть к внутренним органам. Мышцам при этом почти ничего не достается, и они начинают уменьшаться в объеме. Правда, снижение мышечной массы при белковой недостаточности заметить трудно — за счет отеков вес может оставаться относительно стабильным или снижаться очень медленно. Зато вы точно заметите другие признаки постепенной атрофии мышечной ткани — слабость и быструю утомляемость. Люди, желающие скорректировать вес, часто отказываются от жиров или белка, но это ошибка. Важно соблюдать баланс: основу правильной диеты составляют мясо, рыба (или продукты с высоким содержанием белка растительного происхождения), крупы и овощи.
Плохое настроение
Белок, помимо всего прочего, важен для синтеза нейромедиатора серотонина. Именно он отвечает за хорошее настроение и стрессоустойчивость. Недостаток серотонина приводит не только к хандре, плаксивости и мрачным мыслям, но и к бессоннице, повышенной тревожности, нервозности и склонности взрываться по пустякам.
Именно он отвечает за хорошее настроение и стрессоустойчивость. Недостаток серотонина приводит не только к хандре, плаксивости и мрачным мыслям, но и к бессоннице, повышенной тревожности, нервозности и склонности взрываться по пустякам.
Комментарии эксперта
Горбачёва Наталья Леонидовна, диабетолог, диетолог, эндокринолог, ведущий специалист сети клиник «Семейная»
«Правильный белковый обмен веществ — баланс между распадом и синтезом белков. Организму должно хватать аминокислот для построения новых соединений. Степень усвоения белка зависит от его происхождения и способа термической обработки. Элемент не способен накапливаться в организме, его излишки выводятся с помощью почек. Поэтому чрезмерное потребление белка негативно сказывается на их состоянии
Причинами нарушений белкового обмена могут стать наследственные заболевания: подагра, а также тяжелые состояния, такие как онкопатологии, следствие радиационного облучения и прочее. Но в большинстве случаев у взрослого человека симптомы нарушения биосинтеза белков говорят о несбалансированном рационе питания.
Но в большинстве случаев у взрослого человека симптомы нарушения биосинтеза белков говорят о несбалансированном рационе питания.
Недостаток белков — актуальная проблема. Одних она настигает при избавлении от лишнего веса, других — при вегетарианстве, а третьих — из-за заболеваний пищеварительной и эндокринной систем. Дефицит белков может не проявляться клинически, но последствия недостатка протеина довольно печальны:
- задержка роста и развития у детей;
- малая мышечная масса;
- сердечно-сосудистые заболевания;
- плохой аппетит;
- вялость, апатия, усталость;
- плохое состояние кожи, волос, ногтей.
Если биосинтез белков нарушен на этапе построения, человек может страдать от белкового отравления. Характерными признаками интоксикации являются поражение печени и почек, нарушения работы ЖКТ. Переизбыток белка влияет на центральную нервную систему вплоть до серьезных поражений при врожденных нарушениях обмена веществ. При ухудшении самочувствия необходимо сдать анализы и получить рекомендации специалиста.»
При ухудшении самочувствия необходимо сдать анализы и получить рекомендации специалиста.»
450106, г.Уфа, ул. Ст. Кувыкина, 96. e-mail: [email protected]
Белок (часть 1)
⠀ Белки являются основным строительным материалом для организма, для работы мышц и иммунной системы. Белки входят в состав всех клеток организма человека и участвуют во всех этапах обмена веществ.
⠀Белки бывают животного и растительного происхождения. В пищеварительном тракте белки при помощи ферментов расщепляются на аминокислоты, из которых потом организм строит «собственные» белки. Основных аминокислот двадцать две. Причем девять из них организм не может вырабатывать самостоятельно и получает их только с пищей.
⠀
⠀1 грамм белка обеспечивает организму 4 ккал.
⠀Усвояемость животных и растительных белков различна:
– так на 98% усваиваются белки, содержащиеся в яйцах и молочных продуктах,
– на 90% — белки рыбы,
– на 70% — белки мяса и птицы,
– на 50% — белки зерновых,
– на 45% — белки бобовых и овощей.
Из-за низкой усвояемости растительных белков и отсутствия в них незаменимых аминокислот, люди, которые полностью отказываются от белков животного происхождения (мяса, рыбы, яиц, молочных продуктов), испытывают недостаток полноценных белков. ⠀Суточная норма потребления белка должна составлять для взрослого человека 1 грамм на 1 килограмм веса. Причем от 70 до 80% должны составлять белки животного происхождения.
Необходимо помнить о функции белков в организме, а они очень важны! В первую очередь это:
– защитная функция– в ответ на проникновение в организм чужеродных белков или микроорганизмов образуются особые белки – антитела, способные связывать и обезвреживать их. Фибрин, образующийся из фибриногена, способствует остановке кровотечений;
– структурная (строительная) – коллаген придает упругость соединительной ткани;
– каталитическая– ферменты, они обладают специфическими каталитическими свойствами, то есть каждый фермент катализирует одну или несколько сходных реакций, например пепсин, расщепляет белки в процессе пищеварения. Известно около 4000 реакций, катализируемых белками;
Известно около 4000 реакций, катализируемых белками;
– транспортная – гемоглобин переносит кислород и транспортирует его ко всем тканям и органам;
– регуляторная – инсулин регулирует уровень глюкозы в крови, гормон роста усиливает рост организма.
⠀⠀Присутствуют ли в вашем рационе белки, какие? Делитесь в комментариях.
Главный врач Николаева И.Е.
Заместитель главного врача по мед.части Ермолаев Е.Н.
Заместитель главного врача по ОМР Камалова В.Р.
Роль белка — Exponenta
Только полноценный высококачественный белок содержит все незаменимые аминокислоты, которые не синтезирует наш организм. В каждой из них важные свойства, которые определяют качество нашей жизни и состояние здоровья:
Изолейцин играет важную роль в формировании мышечной ткани, служит источником энергии для ее клеток. Способствует увеличению выносливости, восполнению затраченной при физической нагрузке энергии, восстановлению мышц, синтезу наружного слоя кожи, регулированию уровня сахара в крови. Дефицит изолейцина выражается в потере мышечной массы, может развиться гипогликемия.
Способствует увеличению выносливости, восполнению затраченной при физической нагрузке энергии, восстановлению мышц, синтезу наружного слоя кожи, регулированию уровня сахара в крови. Дефицит изолейцина выражается в потере мышечной массы, может развиться гипогликемия.
Лейцин предотвращает усталость, способствует укреплению иммунной системы, повышению работоспособности, увеличению мышечной массы. Понижает содержание сахара в крови и способствует быстрейшему заживлению ран и костей. Недостаток лейцина является причиной нарушения обмена веществ, ослабления иммунитета, быстрого утомления, патологических процессов почках и щитовидной железе.
Лизин – участвует в образовании коллагена и восстановлении тканей, а также выработке антител, гормонов и ферментов. Имеет противовирусное действие, способствует повышению иммунитета. Дефицит приводит к утомляемости, усталости и слабости, неспособности к концентрации, раздражительности, потере волос, головокружение.
Метионин способствует укреплению структуры ногтей и волос, укреплению иммунитета, предотвращению жировых отложений в печени.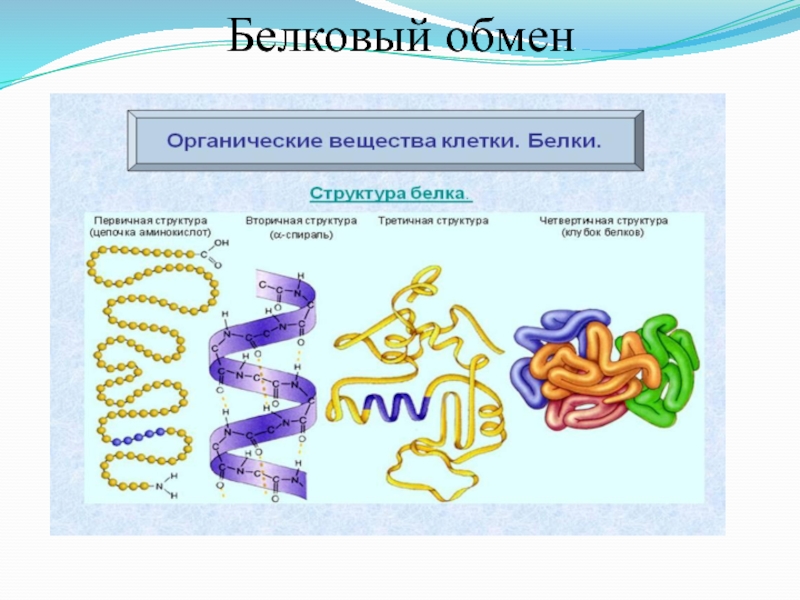 Ускоряет регенеративные процессы, участвует в выводе тяжелых металлов из организма. Недостаток метионина сопровождается серьезным нарушением обмена веществ, является причиной поражения печени.
Ускоряет регенеративные процессы, участвует в выводе тяжелых металлов из организма. Недостаток метионина сопровождается серьезным нарушением обмена веществ, является причиной поражения печени.
Валин служит источником энергии в мышечных клетках, препятствует снижению уровня серотонина. Используется для лечения депрессий и множественного склероза.
Треонин участвует в синтезе иммуноглобулинов и антител, способствует ускорению метаболических процессов в организме, выработке антител, прочности и упругости соединительных тканей и мышц, принимает участие в создании коллагена, эластина и мышечной ткани. Недостаток треонина в организме человека может проявляться такими симптомами, как мышечная слабость, нарушение концентрации внимания, потеря мышечной массы, задержка роста и развития, депрессия.
Фенилаланин способствует регулированию скорости обмена веществ, улучшению ментальной концентрации, регуляции аппетита. Недостаток фенилаланина в организме может привести к потере мышечной массы, гормональным сбоям, нарушению работы щитовидной железы и надпочечников, понижению умственной способности.
Аргинин — частично незаменимая аминокислота, которая играет важную роль в улучшении обменных процессов, стимулирует синтез соматотропного гормона, ускоряет метаболизм жиров и снижает концентрацию холестерина в крови. Недостаток приводит к возрастанию риска развития тромбов, нарушению мозговой деятельности, раннему старению, ожирению, атеросклерозам и гипертонии.
Гистидин — частично незаменимая аминокислота, которая играет важную роль в метаболизме белков, синтезе гемоглобина, красных и белых кровяных телец, является одним из регуляторов свертывания крови. Используется при лечении аллергий, предотвращает псориаз, экзему, нейродермиты. Недостаток приводит к нарушению обмена веществ, торможению синтеза гемоглобина, ослаблению слуха.
Триптофан в организме человека непосредственно преобразуется в серотонин, соединение, которое вызывает умственное расслабление и создает ощущение эмоционального благополучия. Триптофан способен уменьшать болевую чувствительность, стимулирует выработку гормона роста, который необходим для увеличения мышечной массы и уменьшения массы жира. Низкое содержание триптофана в организме вызывает депрессию, тревожность, бессонницу, расстройства внимания, гиперактивность, головные боли.
Низкое содержание триптофана в организме вызывает депрессию, тревожность, бессонницу, расстройства внимания, гиперактивность, головные боли.
белки — урок. Биология, Общие биологические закономерности (9–11 класс).
Белки (протеины, полипептиды) — самые многочисленные, наиболее разнообразные и имеющие первостепенное значение биополимеры. В состав молекул белков входят атомы углерода, кислорода, водорода, азота и иногда серы, фосфора и железа.
Мономерами белков являются аминокислоты, которые (имея в своём составе карбоксильную и аминогруппы) обладают свойствами кислоты и основания (амфотерны).
Благодаря этому аминокислоты могут соединяться друг с другом (их количество в одной молекуле может достигать нескольких сотен). В связи с этим молекулы белков имеют большие размеры, и их называют макромолекулами.
Структура белковой молекулы
Под структурой белковой молекулы понимают её аминокислотный состав, последовательность мономеров и степень скрученности молекулы белка.
В молекулах белков встречается всего \(20\) видов различных аминокислот, и огромное разнообразие белков создаётся за счёт различного их сочетания.
- Последовательность аминокислот в составе полипептидной цепи — это первичная структура белка. Она уникальна для любого типа белка и определяет форму его молекулы, его свойства и функции.
- Длинная молекула белка сворачивается и приобретает сначала вид спирали в результате образования водородных связей между —СО и —NН группами разных аминокислотных остатков полипептидной цепи (между углеродом карбоксильной группы одной аминокислоты и азотом аминогруппы другой аминокислоты). Эта спираль — вторичная структура белка.
- Третичная структура белка — трёхмерная пространственная «упаковка» полипептидной цепи в виде глобулы (шарика). Прочность третичной структуры обеспечивается разнообразными связями, возникающими между радикалами аминокислот (гидрофобными, водородными, ионными и дисульфидными S–S связями).

- Некоторые белки (например, гемоглобин крови человека) имеют четвертичную структуру. Она возникает в результате соединения нескольких макромолекул с третичной структурой в сложный комплекс. Четвертичная структура удерживается непрочными ионными, водородными и гидрофобными связями.
Структура белков может нарушаться (подвергаться денатурации) при нагревании, обработке некоторыми химическими веществами, облучении и др. При слабом воздействии распадается только четвертичная структура, при более сильном — третичная, а затем — вторичная, и белок остаётся в виде полипептидной цепи. В результате денатурации белок теряет способность выполнять свою функцию.
Нарушение четвертичной, третичной и вторичной структур обратимо. Этот процесс называют ренатурацией.
Разрушение первичной структуры необратимо.
Кроме простых белков, состоящих только из аминокислот, есть ещё и сложные белки, в состав которых могут входить углеводы (гликопротеины), жиры (липопротеины), нуклеиновые кислоты (нуклеопротеины) и др.
Функции белков
- Каталитическая (ферментативная) функция. Специальные белки — ферменты — способны ускорять биохимические реакции в клетке в десятки и сотни миллионов раз. Каждый фермент ускоряет одну и только одну реакцию. В состав ферментов входят витамины.
- Структурная (строительная) функция — одна из основных функций белков (белки входят в состав клеточных мембран; белок кератин образует волосы и ногти; белки коллаген и эластин — хрящи и сухожилия).
- Транспортная функция — белки обеспечивают активный транспорт ионов через клеточные мембраны (транспортные белки в наружной мембране клеток), транспорт кислорода и углекислого газа (гемоглобин крови и миоглобин в мышцах), транспорт жирных кислот (белки сыворотки крови способствуют переносу липидов и жирных кислот, различных биологически активных веществ).
- Сигнальная функция. Приём сигналов из внешней среды и передача информации в клетку происходит за счёт встроенных в мембрану белков, способных изменять свою третичную структуру в ответ на действие факторов внешней среды.

- Сократительная (двигательная) функция — обеспечивается сократительными белками — актином и миозином (благодаря сократительным белкам двигаются реснички и жгутики у простейших, перемещаются хромосомы при делении клетки, сокращаются мышцы у многоклеточных, совершенствуются другие виды движения у живых организмов).
- Защитная функция — антитела обеспечивают иммунную защиту организма; фибриноген и фибрин защищают организм от кровопотерь, образуя тромб.
- Регуляторная функция присуща белкам — гормонам (не все гормоны являются белками!). Они поддерживают постоянные концентрации веществ в крови и клетках, участвуют в росте, размножении и других жизненно важных процессах (например, инсулин регулирует содержание сахара в крови).
- Энергетическая функция — при длительном голодании белки могут использоваться в качестве дополнительного источника энергии после того, как израсходованы углеводы и жиры (при полном расщеплении \(1\) г белка до конечных продуктов выделяется \(17,6\) кДж энергии).
 Аминокислоты, высвобождающиеся при расщеплении белковых молекул, используются для построения новых белков.
Аминокислоты, высвобождающиеся при расщеплении белковых молекул, используются для построения новых белков.
Источники:
Каменский А. А., Криксунов Е. А., Пасечник В. В. Биология. 9 класс // ДРОФА.
Каменский А. А., Криксунов Е. А., Пасечник В. В. Биология. Общая биология (базовый уровень) 10–11 класс // ДРОФА.
Лернер Г. И. Биология: Полный справочник для подготовки к ЕГЭ: АСТ, Астрель.
http://ours-nature.ru/lib/b/book/1063747118/348
Синтез белков для безопасной медицины. Как уменьшить побочные эффекты лекарств
Анастасия ГУСАЧ, сотрудник лаборатории структурной биологии рецепторов, сопряженных с G-белком, МФТИ:
— Сейчас мы находимся в лаборатории структурных исследований рецепторов, сопряженных с G-белком, в МФТИ. Наша лаборатория является достаточно молодой. Она появилась всего пять лет назад, но за это короткое время мы успели довести почти до конца уже много важных и значимых на мировом уровне проектов. Сейчас я расскажу немного о том проекте, которым занимаюсь лично.
Этот проект связан со структурными исследованиями рецепторов, связанных с воспалением. Для чего это нужно? Структуры высокого разрешения GPCR позволяют создавать высокоспецифичные лекарства, которые будут иметь минимум побочных эффектов. Побочные эффекты у лекарств возникают из-за того, что эти лекарства недостаточно специфичны. Т.е. они могут взаимодействовать как с целевым белком, так и с различными другими белками. Если мы, например, хотим создать лекарство для блокировки, блокады боли, а наше лекарство будет еще взаимодействовать с рецепторами, отвечающими за воспаление, то мы можем получить не только блокаду боли, но и воспаление, что является побочным эффектом. Мы этого не хотим. Поэтому мы желаем знать структуру нашего целевого рецептора с максимальным (т.е. атомным) разрешением. И после этого мы посмотрим на него, посмотрим на все остальные рецепторы и решим, чем же он такой особенный и как нам сделать лекарство, которое будет ориентировано только на него. Это задача медицины нового поколения. Сейчас она является очень актуальной.
Сейчас она является очень актуальной.
Метод, который позволяет получать структуры белков с максимальным разрешением, на данный момент — это рентгеноструктурный анализ кристаллов белка. Однако белки, на самом деле, не хотят вставать в кристаллы. Они в наших клетках существуют просто в виде единичных молекул либо в виде комплексов. Мы изучаем мембранные белки, к примеру. Они встроены в мембрану. Нам нужно каким-то образом заставить их вставать в кристалл. Для того чтобы просветить их рентгеном и получить усиленную картинку дифракции, потому что картину дифракции от одной молекулы мы не отличим — у нее будет слишком маленькая интенсивность. А если таких молекул будет стоять очень много и в одинаковой ориентации, то интенсивность рассеяния данной молекулы будет увеличена во много-много раз. И мы сможем увидеть картинку дифракции, по которой мы восстановим первоначальную структуру молекулы.
Так вот, вся эта история начинается с производства белка, который пригоден для кристалла. Всем известно, что в нашем организме ДНК кодирует все белки, из которых мы состоим. Поэтому для того, чтобы изменить белки, нам нужно изменить последовательность ДНК. Мы хотим изменить наши белки таким образом, чтобы повысить вероятность кристаллизации. Поэтому на уровне ДНК мы должны сделать какие-то изменения. Мы вносим какие-то мутации: мы можем укоротить белок либо удлинить его. При этом всегда в последующем шаге мы контролируем то, что данный белок до сих пор функционален. Так вот, мы хотим сделать белок — мы берем последовательность ДНК и отдаем ее в клетки так, чтобы эти клетки затем произвели в большом количестве наш белок. Для этого в нашей лаборатории используются клетки насекомых. Также возможно использовать клетки человека (различные клеточные линии), клетки дрожжей, клетки бактерий. Но в случае наших белков GPCR нам нужны клетки эукариот, чтобы правильным образом фолдировать белки (которые при этом наиболее просты в работе).
Всем известно, что в нашем организме ДНК кодирует все белки, из которых мы состоим. Поэтому для того, чтобы изменить белки, нам нужно изменить последовательность ДНК. Мы хотим изменить наши белки таким образом, чтобы повысить вероятность кристаллизации. Поэтому на уровне ДНК мы должны сделать какие-то изменения. Мы вносим какие-то мутации: мы можем укоротить белок либо удлинить его. При этом всегда в последующем шаге мы контролируем то, что данный белок до сих пор функционален. Так вот, мы хотим сделать белок — мы берем последовательность ДНК и отдаем ее в клетки так, чтобы эти клетки затем произвели в большом количестве наш белок. Для этого в нашей лаборатории используются клетки насекомых. Также возможно использовать клетки человека (различные клеточные линии), клетки дрожжей, клетки бактерий. Но в случае наших белков GPCR нам нужны клетки эукариот, чтобы правильным образом фолдировать белки (которые при этом наиболее просты в работе).
Поэтому мы используем яйцеклетки насекомых, которые мы выращиваем в специальной комнате, где поддерживаются максимально «чистые», стерильные условия. Мы используем специальные шейкеры и производим наш белок в этих клетках. После того как мы сделали белок в клетках, мы должны его каким-то образом извлечь. Наш белок мембранный, поэтому нам его надо каким-либо образом добыть из клеточной мембраны. Для этого мы можем использовать такие молекулы, которые называются детергенты. По сути, это то же самое мыло, которое мы используем в быту для того, чтобы растворить жир, который у нас находится на посуде или еще где-то. Ведь клеточная мембрана состоит из липидов, что, по сути, тот же самый жир. Мы должны его удалить, и тогда мы получим наши целевые белки GPCR, силлабилизированные (как это называется по-научному), т.е. в растворенной в молекулах детергента форме.
Мы используем специальные шейкеры и производим наш белок в этих клетках. После того как мы сделали белок в клетках, мы должны его каким-то образом извлечь. Наш белок мембранный, поэтому нам его надо каким-либо образом добыть из клеточной мембраны. Для этого мы можем использовать такие молекулы, которые называются детергенты. По сути, это то же самое мыло, которое мы используем в быту для того, чтобы растворить жир, который у нас находится на посуде или еще где-то. Ведь клеточная мембрана состоит из липидов, что, по сути, тот же самый жир. Мы должны его удалить, и тогда мы получим наши целевые белки GPCR, силлабилизированные (как это называется по-научному), т.е. в растворенной в молекулах детергента форме.
После этого мы их концентрируем в очищенном виде и кристаллизуем. Для этого есть целый инструментарий методов — чтобы работать с мембранными белками. Мы используем т.н. липидную кубическую фазу, которая мимикрирует под нативную мембрану клетки. Таким образом, это может заменять нашему белку его природное окружение. Он себя чувствует комфортно, если можно так выразиться, и собирается в кристаллы. Эти кристаллы мы выращиваем в 96-луночных маленьких плашках. С помощью различных роботов мы подбираем условия кристаллизации. Затем с помощью специальных имиджеров мы ранжируем кристаллы по качеству — визуально и с помощью методов флуоресценции. Затем мы их везем на источник синхротронного излучения. Мы сотрудничаем со многими лабораториями мира — это Франция, Германия, США, Корея и др. Там мы тестируем наши кристаллы на очень мощных источниках рентгена (X-Ray) и получаем картины дифракции.
Он себя чувствует комфортно, если можно так выразиться, и собирается в кристаллы. Эти кристаллы мы выращиваем в 96-луночных маленьких плашках. С помощью различных роботов мы подбираем условия кристаллизации. Затем с помощью специальных имиджеров мы ранжируем кристаллы по качеству — визуально и с помощью методов флуоресценции. Затем мы их везем на источник синхротронного излучения. Мы сотрудничаем со многими лабораториями мира — это Франция, Германия, США, Корея и др. Там мы тестируем наши кристаллы на очень мощных источниках рентгена (X-Ray) и получаем картины дифракции.
Затем ребята, которые специализируются в обработке данных, обрабатывают данные картины дифракции и с помощью разных методов получают те самые искомые структуры высокого разрешения в комплексе с какими-то лигандами. Лигандами для G-белок-сопряженных рецепторов являются различные малые молекулы. Также ими могут быть белковые молекулы или какие-то гормоны. Смысл в том, что клетке нужно как-то узнавать о том, что к ней пришла сигнальная молекула. Она должна как-то на это реагировать. Такими передатчиками этого сигнала как раз являются G-белок-сопряженные рецепторы. Когда вы, например, испугались и у вас выделился адреналин, это вещество взаимодействует с адренергическим рецептором, говоря клетке о том, что нечто произошло и нужно срочно реагировать. Посредством изменения конформации нашего рецептора передается сигнал внутрь клетки, происходит какое-то событие — например, выброс кальция или еще какое-то клеточное событие, которое уже дальше вызывает огромный каскад реакций, который происходит внутри клетки и приводит к клеточному ответу. Вот тем самым «бутылочным горлышком», которое передает сигнал от маленькой молекулы к целой большой клетке, является как раз наш рецептор.
Она должна как-то на это реагировать. Такими передатчиками этого сигнала как раз являются G-белок-сопряженные рецепторы. Когда вы, например, испугались и у вас выделился адреналин, это вещество взаимодействует с адренергическим рецептором, говоря клетке о том, что нечто произошло и нужно срочно реагировать. Посредством изменения конформации нашего рецептора передается сигнал внутрь клетки, происходит какое-то событие — например, выброс кальция или еще какое-то клеточное событие, которое уже дальше вызывает огромный каскад реакций, который происходит внутри клетки и приводит к клеточному ответу. Вот тем самым «бутылочным горлышком», которое передает сигнал от маленькой молекулы к целой большой клетке, является как раз наш рецептор.
На данный момент наши исследования уже находятся на стадии структур и функциональных тестов. Я еще скажу пару фраз о том, зачем нам нужны функциональные тесты. Когда мы кристаллизовали наши рецепторы, мы их как-то изменяли для того, чтобы они закристаллизовались. Но ведь нам нужны структуры тех самых первых рецепторов, которые есть у нас в организме, а не тех рецепторов, которые мы поменяли для того, чтобы было легче с ними работать. Нам нужно убедиться, что наши закристаллизованные рецепторы аналогичны по функциональным свойствам рецепторам дикого типа. Поэтому мы делаем различные тесты, где мы сравниваем первоначальный рецептор и закристаллизованный рецептор. Мы видим, что на самом деле, несмотря на то что мы внесли модификации, они реагируют на лиганды одинаково. Они одинаково себя ведут в клетке. И поэтому мы можем с хорошей степенью уверенности сказать, что это та самая структура, которая нужна для разработки лекарств. И сейчас мы уже думаем про то, как наши структуры помогут в создании новых лекарств для наших целевых рецепторов. Мы надеемся, что это поможет в будущем разработке лекарств.
Но ведь нам нужны структуры тех самых первых рецепторов, которые есть у нас в организме, а не тех рецепторов, которые мы поменяли для того, чтобы было легче с ними работать. Нам нужно убедиться, что наши закристаллизованные рецепторы аналогичны по функциональным свойствам рецепторам дикого типа. Поэтому мы делаем различные тесты, где мы сравниваем первоначальный рецептор и закристаллизованный рецептор. Мы видим, что на самом деле, несмотря на то что мы внесли модификации, они реагируют на лиганды одинаково. Они одинаково себя ведут в клетке. И поэтому мы можем с хорошей степенью уверенности сказать, что это та самая структура, которая нужна для разработки лекарств. И сейчас мы уже думаем про то, как наши структуры помогут в создании новых лекарств для наших целевых рецепторов. Мы надеемся, что это поможет в будущем разработке лекарств.
Редакция «Чердака»
Основы правильного питания — Школа здоровья — ГБУЗ Городская поликлиника 25 г. Краснодара МЗ КК
25 сентября 2019 г.
Значение белков, жиров и углеводов (БЖУ) в питании человека
Значение белка в питании здорового человека
Белки – сложные азотсодержащие биополимеры, мономерами которых служат α-аминокислоты. Белки – высокомолекулярные соединения. Их молекулярная масса колеблется от 6000 до 100000 и более. Аминокислотный состав различных белков неодинаков и является важнейшей характеристикой каждого белка, а также критерием его ценности в питании. Аминокислоты – органические соединения, в которых имеются две функциональные группы – карбоксильная, определяющая кислотные свойства молекул и аминогруппа, придающая этим соединениям основные свойства.
Среди большого число природных аминокислот в составе белков с наибольшим постоянством обнаруживают следующие 20 аминокислот: глицин (гликокол), аланин, серин, треонин, метионин, цистин, валин, лейцин, изолейцин, глутаминовая кислота, глутамин, аспарагиновая кислота, аспарагин, аргинин, лизин, фенилаланин, тирозин, гистидин, триптофан, пролин.
Все белки принято делить на простые (протеины) и сложные (протеиды). Под простыми понимают соединения, включающие в свой состав лишь полипептидные цепи, под сложными белками – соединения, в которых наряду с белковой молекулой имеется также небелковая часть – так называемая простетическая группа. В зависимости от пространственной структуры белки можно разделить на глобулярные и фибриллярные. К числу простых глобулярных белков относятся, в частности, альбумины, глобулины, проламины и глютелины. Альбумины и глобулины широко распространены в природе и составляют основную часть белков сыворотки крови, молока и яичного белка. Проламины и глютелины относятся к растительным белкам и встречаются в семенах злаков, образуя основную массу клейковины. Эти белки нерастворимы в воде. К проламин относятся глиадин пшеницы, зеин кукурузы, гордеин ячменя. Аминокислотный состав этих белков характеризуется низким содержанием лизина, а также треонина, метионина и триптофана и чрезвычайно высоким – глутаминовой кислоты.
Представители структурных белков, так называемые протеиноиды, являются фибриллярными белками главным образом животного происхождения. Эти белки выполняют в организме опорную функцию. Они нерастворимы в воде и весьма устойчивы к перевариванию пищеварительными ферментами. К ним относятся кератины (белки волос, ногтей, эпидермиса), эластин (белок связок, соединительной ткани сосудов и мышц), коллаген (белок костной, хрящевой, рыхлой и плотной соединительной ткани). При длительном кипячении в воде коллаген превращается в водорастворимый белок – желатин (глютин). Коллаген содержит значительное количество необычных для других белков аминокислот оксипролина и оксилизина, но в нем отсутствует триптофан.
Основные функции белков в организме.
1. П л а с т и ч е с к а я. Белки составляют 15-20% сырой массы различных тканей (в сравнении – липиды и углеводы лишь 1-5%) и являются основным строительным материалом клетки, ее органоидов и межклеточного вещества. Белки наряду с фосфолипидами образуют остов всех биологических мембран, играющих важную роль в построении клеток и их функционировании.
Белки наряду с фосфолипидами образуют остов всех биологических мембран, играющих важную роль в построении клеток и их функционировании.
2. К а т а л и т и ч е с к а я. Белки являются основным компонентом всех без исключения известных в настоящее время ферментов. При этом простые ферменты представляют собой чисто белковые соединения. В построении сложных ферментов наряду с молекулами белка участвуют и низкомолекулярные соединения (коферменты). Ферментам принадлежит решающая роль в ассимиляции пищевых веществ организмом человека и в регуляции всех внутриклеточных обменных процессов.
3. Г о р м о н а л ь н а я. Значительная часть гормонов по своей природе является белками или полипептидами. К их числу принадлежит инсулин, гормоны гипофиза (АКТГ, соматотропный, тиреотропный и др.), паратиреоидный гормон.
4. Ф у н к ц и я с п е ц и ф и ч н о с т и. Чрезвычайное разнообразие и уникальность индивидуальных белков обеспечивают тканевую индивидуальную и видовую специфичность, лежащую в основе проявлений иммунитета и аллергии. В ответ на поступление в организм чужеродных для него белков – антигенов – в иммунокомпетентных органах и клетках происходит активный синтез антител, представляющих особый вид глобулинов (иммуноглобулины). Специфическое взаимодействие антигена с соответствующими антителами составляет основу иммунных реакций, обеспечивающих защиту организма от чужеродных агентов.
В ответ на поступление в организм чужеродных для него белков – антигенов – в иммунокомпетентных органах и клетках происходит активный синтез антител, представляющих особый вид глобулинов (иммуноглобулины). Специфическое взаимодействие антигена с соответствующими антителами составляет основу иммунных реакций, обеспечивающих защиту организма от чужеродных агентов.
5. Т р а н с п о р т н а я. Белки участвуют в транспорте кровью кислорода (Hb), липидов (липопротеиды), углеводов (гликопротеиды), некоторых витаминов, гормонов, лекарственных веществ и др. Вместе с тем специфические белки-переносчики обеспечивают транспорт различных минеральных солей и витаминов через мембраны клеток и субклеточных структур.
Белки организма – чрезвычайно динамичные структуры, постоянно обновляющие свой состав вследствие непрерывно протекающих и тесно сопряженных друг с другом процессов их распада и синтеза. Организм человека практически лишен резерва белка, причем углеводы и жиры также не могут служить его предшественниками. В связи с этим единственным источником пополнения фонда аминокислот и обеспечения равновесия процессов синтеза и распада белков в организме могут служить пищевые белки, являющиеся вследствие этого незаменимыми компонентами пищевого рациона.
В связи с этим единственным источником пополнения фонда аминокислот и обеспечения равновесия процессов синтеза и распада белков в организме могут служить пищевые белки, являющиеся вследствие этого незаменимыми компонентами пищевого рациона.
Белки, содержащиеся в пищевых продуктах, не могут однако, непосредственно усваиваться организмом и должны быть предварительно расщеплены в желудочно-кишечном тракте до составляющих их аминокислот, из которых организм формирует характерные для него белковые молекулы. Из 20 аминокислот, образующихся при гидролизе белков, 8 (валин, лейцин, изолейцин, треонин, фенилаланин, триптофан, метионин, лизин) не синтезируются в организме человека и поэтому являются незаменимыми факторами питания. Для детей в возрасте до года незаменимой аминокислотой служит также гистидин. Другие 11 аминокислот могут претерпевать в организме взаимопревращения и не являются незаменимыми. Поскольку для построения подавляющего большинства белков организма человека требуются все 20 аминокислот, но в различных соотношениях, дефицит любой из незаменимых аминокислот в пищевом рационе неизбежно ведет к нарушению синтеза белков.
При нарушении сбалансированности аминокислотного состава рациона синтез полноценных белков также нарушается, что ведет к возникновению ряда патологических изменений. В связи с этим пищевые белки следует рассматривать, прежде всего, как поставщики в организм человека незаменимых аминокислот. Наряду с использованием для синтеза белковых молекул аминокислоты могут окисляться в организме и служить источником энергии. Конечными продуктами катаболизма аминокислот являются углекислый газ, вода и аммиак, который выводится из организма в виде мочевины и некоторых других менее токсичных соединений.
Недостаточное поступление с пищей белков нарушает динамическое равновесие процессов белкового анаболизма и катаболизма, сдвигая его в сторону преобладания распада собственных белков организма, в том числе и белков ферментов.
Избыточное поступление пищевых белков также небезразлично для организма. Оно вызывает усиленную работу пищеварительного аппарата, значительную активацию процессов межуточного обмена аминокислот и синтеза мочевины, увеличивает нагрузку на клубочковый и канальцевый аппарат почек, связанную с усиленной экскрецией конечных продуктов азотистого обмена. При этом может возникать перенапряжение указанных процессов с их последующим функциональным истощением. Избыточное поступление в организм белков может также вести к образованию в желудочно-кишечном тракте продуктов их гниения и неполного расщепления, способных вызывать интоксикацию человека.
При этом может возникать перенапряжение указанных процессов с их последующим функциональным истощением. Избыточное поступление в организм белков может также вести к образованию в желудочно-кишечном тракте продуктов их гниения и неполного расщепления, способных вызывать интоксикацию человека.
Важным показателем качества пищевого белка может служить и степень его усвояемости, которая объединяет протеолиз в желудочно-кишечном тракте и последующее всасывание аминокислот. По скорости переваривания протеолитическими ферментами пищевые белки можно расположить в следующей последовательности: 1) рыбные и молочные, 2) мясные, 3) белки хлеба и круп.
Хлеб и хлебобулочные изделия, крупы и макаронные изделия содержат 5-12% белка; с учетом значительного потребления этих продуктов жителями нашей страны они вносят весьма существенный вклад в обеспечение человека белком. Однако белок хлебобулочных изделий и круп дефицитен по ряду аминокислот, в первую очередь по лизину, и не является достаточно полноценным.
Как коронавирус заражает организм (схема)
Коронавирус SARS-CoV-2 ранее 2019-nCoV, вирус, вызывающий коронавирусную инфекцию (COVID-19), в настоящее время распространяется по всему миру. Известно, что по меньшей мере шесть других типов коронавируса заражают людей, причем некоторые вызывают простуду, а две вызывают эпидемии: атипичная пневмония в 2002 году и MERS в 2012 году.
Покрыты шипами
Коронавирус назван в честь короноподобных шипов, выступающих из его поверхности. Вирус заключен в пузырек маслянистых липидных молекул, который распадается при контакте с мылом.
Вход в уязвимую клетку
Вирус попадает в организм через нос, рот или глаза, а затем прикрепляется к клеткам дыхательных путей, которые продуцируют белок, называемый ACE2. Считается, что вирус возник у летучих мышей, где он мог присоединиться к аналогичному белку.
Высвобождение вирусной РНК
Вирус заражает клетку, сливая ее масляную мембрану с мембраной клетки. Оказавшись внутри, коронавирус высвобождает фрагмент генетического материала под названием РНК.
Оказавшись внутри, коронавирус высвобождает фрагмент генетического материала под названием РНК.
Освобождение камеры
Геном вируса имеет длину менее 30 000 генетических «букв». (У нас более 3 миллиардов.) Зараженная клетка считывает РНК и начинает производить белки, которые будут держать иммунную систему в страхе и помогут собрать новые копии вируса.
Антибиотики убивают бактерии и не действуют против вирусов. Но исследователи тестируют антивирусные препараты, которые могут разрушить вирусные белки и остановить инфекцию.
Создание вирусных белков
По мере прогрессирования инфекции механизм клетки начинает производить новые спайки и другие белки, которые будут образовывать больше копий коронавируса.
Сборка новых копий
Новые копии вируса собираются и переносятся на внешние края клетки.
Распространение инфекции
Каждая зараженная клетка может выпустить миллионы копий вируса, прежде чем клетка окончательно разрушится и умрет. Вирусы могут инфицировать близлежащие клетки или попасть в капли, которые покидают легкие.
Иммунная реакция
Большинство инфекций Covid-19 вызывают лихорадку, поскольку иммунная система борется, чтобы очистить вирус. В тяжелых случаях иммунная система может чрезмерно реагировать и начать атаковать клетки легких. Легкие закупориваются жидкостью и отмирающими клетками, что затрудняет дыхание. Небольшой процент инфекций может привести к острому респираторному дистресс-синдрому и, возможно, смерти.
Покидая тело
Кашель и чихание могут привести к попаданию вирусных капель на находящихся поблизости людей и поверхности, где вирус может оставаться заразным от нескольких часов до нескольких дней. Зараженные люди могут избежать распространения вируса, надев маску, но здоровым людям не нужно носить маску, если они не заботятся о больном человеке.
Как быть с возможной вакциной
Будущая вакцина может помочь организму вырабатывать антитела, которые нацелены на вирус SARS-CoV-2 и предотвращают его заражение человеческими клетками. Вакцина против гриппа работает аналогичным образом, но антитела, полученные из вакцины против гриппа, не защищают от коронавируса.
Лучший способ избежать заражения коронавирусом и другими вирусами — мыть руки с мылом, избегать прикосновения к лицу, держаться подальше от больных людей и регулярно чистить часто используемые поверхности.
Источники: доктор Мэтью Б. Фриман и доктор Стюарт Уэстон, Univ. Мэрилендской Школы Медицины; Поля вирусологии; Медицинская вирусология Феннера и Уайта; Природа; Наука; Ланцет; Медицинский журнал Новой Англии; Центры по контролю и профилактике заболеваний.
https://www.nytimes.com/interactive/2020/03/11/science/how-coronavirus-hijacks-your-cells.html
Объяснитель: Что такое белки? | Новости науки для студентов
аминокислот Простые молекулы, которые естественным образом встречаются в тканях растений и животных и являются основными строительными блоками белков.
клетка Наименьшая структурная и функциональная единица организма. Обычно он слишком мал, чтобы увидеть невооруженным глазом, он состоит из водянистой жидкости, окруженной мембраной или стенкой. В зависимости от размера животные состоят из тысяч или триллионов клеток.Большинство организмов, таких как дрожжи, плесень, бактерии и некоторые водоросли, состоят только из одной клетки.
химический Вещество, состоящее из двух или более атомов, которые объединяются (связываются) в фиксированной пропорции и структуре. Например, вода — это химическое вещество, которое образуется, когда два атома водорода связываются с одним атомом кислорода. Его химическая формула — H 2 O. Химический также может быть прилагательным для описания свойств материалов, которые являются результатом различных реакций между различными соединениями.
коллаген Волокнистый белок, содержащийся в костях, хрящах, сухожилиях и других соединительных тканях.
компонент Что-то, что является частью чего-то еще (например, элементы, которые помещаются на электронной плате, или ингредиенты, которые входят в рецепт печенья).
диета (прил. диета ) Пища и жидкости, потребляемые животным для обеспечения питания, необходимого для роста и поддержания здоровья.
растворить Превратить твердое вещество в жидкость и диспергировать его в исходной жидкости.(Например, твердые кристаллы сахара или соли растворятся в воде. Теперь кристаллы исчезли, и раствор представляет собой полностью диспергированную смесь жидкой формы сахара или соли в воде.)
ДНК (сокращение от дезоксирибонуклеиновой кислоты) Длинная, двухцепочечная и спиралевидная молекула внутри большинства живых клеток, несущая генетические инструкции. Он построен на основе атомов фосфора, кислорода и углерода. Эти инструкции сообщают клеткам, какие молекулы должны образовывать все живые существа, от растений и животных до микробов.
ген (прил. Генетический) Сегмент ДНК, который кодирует или содержит инструкции для производства белка клеткой. Потомство наследует гены от родителей. Гены влияют на внешний вид и поведение организма.
мышца Тип ткани, используемый для движения путем сокращения своих клеток, известный как мышечные волокна. Мышцы богаты белком, поэтому хищные виды ищут добычу, содержащую много этой ткани.
арахис Не настоящий орех (который растет на деревьях), эти богатые белком семена на самом деле являются бобовыми.Они принадлежат к семейству растений семейства гороховых и бобовых и растут в стручках под землей.
пептид Короткая цепочка аминокислот (обычно менее 100).
белок Соединение, состоящее из одной или нескольких длинных цепочек аминокислот. Белки — неотъемлемая часть всех живых организмов. Они составляют основу живых клеток, мышц и тканей; они также выполняют работу внутри клеток. Среди наиболее известных автономных белков — гемоглобин (в крови) и антитела (также в крови), которые пытаются бороться с инфекциями.Лекарства часто работают, удерживая белки.
ткань Состоит из клеток, представляет собой любой из отдельных типов материалов, из которых состоят животные, растения или грибы. Клетки внутри ткани работают как единое целое, выполняя определенную функцию в живых организмах. Например, разные органы человеческого тела часто состоят из разных типов тканей.
виджет В информатике — инструмент, встроенный в программу или веб-сайт, который позволяет пользователю выполнять действия в ответ на информацию, отображаемую на экране.
Производство белка — Принципы биологии
Белки — одна из самых распространенных органических молекул в живых системах, обладающая невероятно разнообразным набором функций. Белки используются для:
- Строить структуры внутри клетки (например, цитоскелет)
- Регулировать производство других белков, контролируя синтез белка
- Проведите по цитоскелету, чтобы вызвать сокращение мышц
- Транспортные молекулы через клеточную мембрану
- Ускорить химические реакции (ферменты)
- Действовать как токсины
Каждая клетка живой системы может содержать тысячи различных белков, каждый из которых выполняет уникальную функцию.Их структуры, как и их функции, сильно различаются. Однако все они представляют собой полимеры аминокислот, расположенных в линейной последовательности ( Рисунок 1 ).
Функции белков очень разнообразны, потому что они состоят из 20 различных химически различных аминокислот, которые образуют длинные цепи, и аминокислоты могут быть в любом порядке. Функция белка зависит от формы белка. Форма белка определяется порядком аминокислот. Белки часто состоят из сотен аминокислот и могут иметь очень сложную форму, потому что существует очень много различных возможных порядков для 20 аминокислот!
Рисунок 1 Структура белка.Цветные шары в верхней части диаграммы представляют собой разные аминокислоты. Аминокислоты — это субъединицы, которые соединяются рибосомой с образованием белка. Затем эта цепочка аминокислот складывается, образуя сложную трехмерную структуру. (Предоставлено: Lady of Hats из Википедии; общественное достояние)Вопреки тому, во что вы можете верить, белки обычно не используются клетками в качестве источника энергии. Белок из вашего рациона расщепляется на отдельные аминокислоты, которые собираются вашими рибосомами в белки, которые нужны вашим клеткам.Рибосомы не производят энергию.
Рисунок 2 Примеры продуктов с высоким содержанием белка. («Белок» Национального института рака находится в открытом доступе)Информация для производства белка закодирована в ДНК клетки. При производстве белка создается копия ДНК (называемая мРНК), и эта копия переносится на рибосому. Рибосомы считывают информацию в мРНК и используют эту информацию для сборки аминокислот в белок. Если белок будет использоваться в цитоплазме клетки, рибосома, создающая белок, будет свободно плавать в цитоплазме.Если белок будет нацелен на лизосому, стать компонентом плазматической мембраны или секретироваться вне клетки, белок будет синтезироваться рибосомой, расположенной на шероховатом эндоплазматическом ретикулуме (RER). После синтеза белок будет перенесен в везикуле от RER к поверхности cis Гольджи (сторона, обращенная внутрь клетки). По мере того, как белок проходит через Гольджи, его можно модифицировать. Как только последний модифицированный белок завершен, он выходит из Гольджи в пузырьке, который отрастает от поверхности trans .Оттуда везикула может быть нацелена на лизосому или на плазматическую мембрану. Если везикула сливается с плазматической мембраной, белок станет частью мембраны или будет выброшен из клетки.
Рисунок 3 Схема эукариотической клетки. (Фото: Медиран, Викимедиа, 14 августа 2002 г.)Инсулин
Инсулин — это белковый гормон, который вырабатывается определенными клетками поджелудочной железы, называемыми бета-клетками. Когда бета-клетки чувствуют, что уровень глюкозы (сахара) в кровотоке высок, они производят белок инсулина и выделяют его вне клеток в кровоток.Инсулин дает клеткам сигнал поглощать сахар из кровотока. Клетки не могут усваивать сахар без инсулина. Белок инсулина сначала образуется в виде незрелой, неактивной цепи аминокислот (препроинсулин — см. Рисунок 4). Он содержит сигнальную последовательность, которая направляет незрелый белок в грубый эндоплазматический ретикулум, где он складывается в правильную форму. Затем нацеливающая последовательность отрезается от аминокислотной цепи с образованием проинсулина. Этот обрезанный, свернутый белок затем отправляется к Гольджи внутри пузырька.В системе Гольджи из белка удаляется больше аминокислот (цепь C), чтобы произвести окончательный зрелый инсулин. Зрелый инсулин хранится в специальных пузырьках до тех пор, пока не будет получен сигнал для его попадания в кровоток.
Рисунок 4 Созревание инсулина. (Фотография предоставлена консорциумом Beta Cell Biology Consortium, Викимедиа. 2004 г. Это изображение находится в открытом доступе.Если не указано иное, изображения на этой странице лицензированы OpenStax в соответствии с CC-BY 4.0.
Текст адаптирован из: OpenStax, Концепции биологии.OpenStax CNX. 18 мая 2016 г. http://cnx.org/contents/[email protected]
Сворачивание белков: хорошее, плохое и уродливое
Мы часто думаем о белках как о питательных веществах в пище, которые мы едим, или как об основном компоненте мышц, но белки также представляют собой микроскопические молекулы внутри клеток, которые выполняют разнообразные и жизненно важные функции. Завершив проект «Геном человека», ученые обращают свое внимание на «протеом» человека — каталог всех человеческих белков. Эта работа показала, что мир белков увлекателен, он полон молекул с такими замысловатыми формами и точными функциями, что они кажутся почти фантастическими.
Функция белка зависит от его формы, и когда образование белка идет не так, образующиеся в результате деформированные белки вызывают проблемы, которые варьируются от плохих, когда белки пренебрегают своей важной работой, до уродливых, когда они образуют липкую комковатую массу внутри клеток. Текущие исследования показывают, что мир белков далек от первозданного. Образование белка — это процесс, подверженный ошибкам, и ошибки на этом пути были связаны с рядом заболеваний человека.
Мир белков:
В типичной человеческой клетке содержится от 20 000 до более чем 100 000 уникальных типов белков.Почему так много? Белки — это рабочие лошадки клетки. Каждый мастерски выполняет определенную задачу. Некоторые из них являются структурными, например, придают жесткость мышечным клеткам или длинным тонким нейронам. Другие связываются с определенными молекулами и доставляют их в новые места, а третьи катализируют реакции, которые позволяют клеткам делиться и расти. Такое разнообразие и специфичность функций стало возможным благодаря, казалось бы, простому свойству белков: они сворачиваются.
Белки складываются в функциональную форму
Белок начинается в клетке как длинная цепочка, состоящая в среднем из 300 строительных блоков, называемых аминокислотами.Существует 22 различных типа аминокислот, и их порядок определяет, как белковая цепь будет складываться сама по себе. При складывании первыми обычно образуются конструкции двух типов. Некоторые области белковой цепи сворачиваются в тонкие образования, называемые «альфа-спиралями», в то время как другие области складываются в зигзагообразные узоры, называемые «бета-листами», которые напоминают складки бумажного веера. Эти две структуры могут взаимодействовать, образуя более сложные структуры. Например, в одной структуре белка несколько бета-листов обвиваются вокруг себя, образуя полую трубку с несколькими альфа-спиралями, выступающими из одного конца.Трубка короткая и приземистая, так что общая структура напоминает змей (альфа-спирали), выходящих из банки (бета-листовая трубка). Несколько других белковых структур с описательными названиями включают «бета-ствол», «бета-пропеллер», «альфа / бета-подкову» и «складку желе-ролла».
Эти сложные структуры позволяют белкам выполнять свою разнообразную работу в клетке. Белок «змеи в банке», будучи встроенным в клеточную мембрану, создает туннель, который позволяет входить и выходить из клеток.Другие белки образуют формы с карманами, называемыми «активными центрами», которые идеально подходят для связывания с определенной молекулой, например, с замком и ключом. Сворачиваясь в различные формы, белки могут выполнять очень разные роли, несмотря на то, что они состоят из одних и тех же основных строительных блоков. Чтобы провести аналогию, все автомобили сделаны из стали, но обтекаемая форма гоночного автомобиля побеждает в гонках, в то время как автобус, самосвал, кран или дзамбони имеют форму для выполнения своих уникальных задач.
Почему иногда происходит сбой сворачивания белка?
Сворачивание позволяет белку принимать функциональную форму, но это сложный процесс, который иногда терпит неудачу.Сворачивание белков может пойти не так по трем основным причинам:
1: Человек может обладать мутацией, которая изменяет аминокислоту в белковой цепи, что затрудняет поиск конкретного белка его предпочтительной складки или «нативного» состояния. Это касается наследственных мутаций, например, приводящих к муковисцидозу или серповидно-клеточной анемии. Эти мутации расположены в последовательности ДНК или «гене», кодирующем один конкретный белок. Следовательно, эти типы унаследованных мутаций влияют только на этот конкретный белок и связанные с ним функции.
2: С другой стороны, нарушение сворачивания белков можно рассматривать как продолжающийся и более общий процесс, который влияет на многие белки. Когда создаются белки, машина, считывающая указания ДНК для создания длинных цепочек аминокислот, может делать ошибки. По оценкам ученых, этот механизм, рибосома, допускает ошибки в 1 из каждых 7 белков! Эти ошибки могут снизить вероятность правильного сворачивания полученных белков.
3: Даже если аминокислотная цепь не имеет мутаций или ошибок, она все равно может не достичь своей предпочтительной складчатой формы просто потому, что белки не складываются правильно в 100% случаев.Сворачивание белка становится еще более трудным, если условия в клетке, такие как кислотность и температура, изменяются от тех, к которым привык организм.
Нарушение сворачивания белка вызывает несколько известных заболеваний, и ученые предполагают, что многие другие болезни могут быть связаны с проблемами сворачивания. Есть две совершенно разные проблемы, которые возникают в клетках, когда их белки не сворачиваются должным образом.
Один тип проблемы, называемый «потеря функции», возникает, когда недостаточное количество определенного белка сворачивается должным образом, вызывая нехватку «специализированных работников», необходимых для выполнения конкретной работы.Например, представьте, что правильно сложенный белок имеет идеальную форму, чтобы связывать токсин и расщеплять его на менее токсичные побочные продукты. Без достаточного количества правильно сложенного белка токсин будет накапливаться до разрушительного уровня. В качестве другого примера, белок может отвечать за метаболизм сахара, так что клетка может использовать его для получения энергии. Клетка будет расти медленно из-за недостатка энергии, если в ее функциональном состоянии будет недостаточно белка. Причина, по которой клетка заболевает, в этих случаях связана с нехваткой одного специфического, правильно сложенного, функционального белка.Муковисцидоз, болезнь Тея-Сакса, синдром Марфана и некоторые формы рака являются примерами заболеваний, которые возникают, когда один тип белка не может выполнять свою работу. Кто знал, что один тип белка из десятков тысяч может быть настолько важен?
Белки, которые сворачиваются неправильно, также могут повлиять на здоровье клетки независимо от функции белка. Когда белки не могут свернуться в свое функциональное состояние, полученные неправильно свернутые белки могут принимать форму, неблагоприятную для переполненной клеточной среды.Большинство белков содержат липкие, «ненавидящие воду» аминокислоты, которые они закапывают глубоко внутри своего ядра. Неправильно свернутые белки носят эти внутренние части снаружи, как леденцы в шоколаде, раздавленные, чтобы обнажить липкую карамельную серединку. Эти неправильно свернутые белки часто слипаются, образуя сгустки, называемые «агрегатами». Ученые предполагают, что накопление неправильно свернутых белков играет роль в нескольких неврологических заболеваниях, включая болезнь Альцгеймера, Паркинсона, Хантингтона и болезнь Лу Герига (БАС), но ученые все еще работают над тем, чтобы точно выяснить, как эти неправильно свернутые липкие молекулы наносят ущерб клеткам. .
Один неправильно свернутый белок выделяется среди остальных и заслуживает особого внимания. «Прионный» белок при болезни Крейтцфельдта-Якоба, также известной как болезнь коровьего бешенства, является примером неправильно свернутого белка. Этот белок не только необратимо неправильно свернут, но и превращает другие функциональные белки в свое скрученное состояние.
Как наши клетки защищаются от неправильно свернутых белков?
Недавние исследования показывают, что неправильная укладка белков часто происходит внутри клеток.К счастью, клетки привыкли справляться с этой проблемой и имеют несколько систем для повторного укладки или разрушения аберрантных белковых образований.
Шапероны — одна из таких систем. Правильно названные, они сопровождают белки в процессе сворачивания, улучшая шансы белка на правильное сворачивание и даже позволяя некоторым неправильно свернутым белкам возможность повторно укладываться. Интересно, что шапероны сами по себе являются белками! Есть много разных типов шаперонов. Некоторые специально предназначены для помощи одному типу белка, в то время как другие действуют более широко.Некоторые шапероны имеют форму больших полых камер и обеспечивают белкам безопасное пространство, изолированное от других молекул, в котором они могут складываться. Производство нескольких шаперонов усиливается, когда клетка сталкивается с высокими температурами или другими условиями, затрудняющими сворачивание белков, в результате чего эти шапероны получили прозвище «белки теплового шока».
Другая линия защиты клеток от неправильно свернутых белков называется протеасомой. Если неправильно свернутые белки задерживаются в клетке, они будут уничтожены этой машиной, которая пережевывает белки и выплевывает их в виде небольших фрагментов аминокислот.Протеасома похожа на центр переработки, позволяющий клетке повторно использовать аминокислоты для производства большего количества белков. Сама протеасома — это не один белок, а множество действующих вместе. Белки часто взаимодействуют с образованием более крупных структур с важными клеточными функциями. Например, хвост спермы человека представляет собой структуру, состоящую из многих типов белков, которые работают вместе, образуя сложный роторный двигатель, который продвигает сперму вперед.
Будущие исследования сворачивания и неправильного сворачивания белков:
Почему некоторые неправильно свернутые белки способны уклоняться от таких систем, как шапероны и протеасома? Как липкие неправильно свернутые белки могут вызывать перечисленные выше нейродегенеративные заболевания? Некоторые белки неправильно складываются чаще, чем другие? Эти вопросы находятся в авангарде текущих исследований, направленных на понимание основ биологии белков и болезней, которые возникают в результате неправильного сворачивания белка.
Обширный мир белков с большим разнообразием форм наделяет клетки способностями, которые позволяют жизни существовать и допускают ее разнообразие (например, различия между клетками глаза, кожи, легких или сердца, а также различия между видами) . Возможно, по этой причине слово «белок» происходит от греческого слова «протас», что означает «первостепенное значение».
–Предоставлено Керри Гейлер, аспирантом 4 курса Гарвардского факультета органической и эволюционной биологии
Новая вселенная мини-протеинов меняет клеточную биологию и генетику | Наука
Митч Лесли,
Мыши посрамляют бегунов-людей. Несмотря на скромные успехи, грызуны могут преодолевать 10 и более километров за ночь на колесе для упражнений. Но выделялись мыши, которых мышечный биолог Эрик Олсон из Юго-Западного медицинского центра Техасского университета в Далласе и его коллеги представили в 2015 году. На беговой дорожке мыши могли суетиться по крутому склону 10% в течение примерно 90 минут, прежде чем споткнуться, что на 31% дольше, чем у других грызунов. Эти железные мыши отличались от своих собратьев только одним маленьким отличием — исследователи генетически изменили животных так, чтобы им не хватало одного мышечного белка.Этого было достаточно, чтобы развязать превосходную мышечную производительность. «Это как будто вы отключили тормоза», — говорит Олсон.
Столь же поразительной была природа важнейшего белка. В мышцах содержится огромное количество белков. Дистрофин, структурный белок, ген которого может нести мутации, вызывающие мышечную дистрофию, содержит более 3600 аминокислот. Титин, который действует как пружина, придавая мышцам эластичность, является крупнейшим известным белком, содержащим более 34 000 аминокислот. Белок, отключенный у мышей, имеет ничтожное значение 46.Хотя исследователи изучали, как работают мышцы более 150 лет, они полностью упустили из виду огромное влияние этого крошечного белка, называемого миорегулин, на функцию мышц.
Не только Олсон и его коллеги были ошеломлены белками лилипутов. Как теперь понимают ученые, их первоначальные правила анализа геномов отличались от идентификации этих молекул размером с пинту. Теперь более широкие критерии и лучшие методы обнаружения позволяют обнаруживать крошечные белки тысячами, не только у мышей, но и у многих других видов, включая человека.«Впервые мы собираемся исследовать эту вселенную новых белков», — говорит биохимик Джонатан Вайсман из Калифорнийского университета в Сан-Франциско.
Биологи только начинают вникать в функции этих молекул, называемых микробелками, микропептидами или минипротеинами. Но их небольшой размер, кажется, позволяет им блокировать сложную работу более крупных белков, подавляя одни клеточные процессы, вызывая при этом другие. Ранние результаты показывают, что микробелки укрепляют иммунную систему, контролируют разрушение дефектных молекул РНК, защищают бактерии от жары и холода, определяют время цветения растений и обеспечивают токсичный удар для многих типов яда.«Вероятно, во всех биологических процессах будут участвовать небольшие [белки]. Мы просто не искали их раньше», — говорит биохимик Алан Сагателиан из Института биологических исследований Солка в Сан-Диего, Калифорния.
Яд этого хищного водяного клопа содержит более десятка мелких белков.
ЭНДРЮ УОКЕРМаленькие белки также обещают пересмотреть текущее понимание генома.Многие из них, по-видимому, закодированы в участках ДНК и РНК, которые, как считалось, не помогают создавать какие-либо белки. Некоторые исследователи предполагают, что короткие участки ДНК могут быть генами новорожденных, которые эволюционируют в более крупные гены, которые производят полноразмерные белки. Отчасти благодаря небольшим белкам, «нам нужно переосмыслить, что такое гены», — говорит микробиолог и молекулярный биолог Гизела Сторц из Национального института здоровья детей и развития человека в Бетесде, штат Мэриленд.
Несмотря на остающуюся загадку, ученые уже исследуют потенциальные возможности использования этих молекул.Одна компания продает инсектициды, полученные из небольших белков яда австралийского воронкообразного паука. В ходе клинических испытаний оценивается агент для визуализации на основе еще одного крошечного белка в яде скорпиона, предназначенный для выделения границ опухолей, чтобы хирурги могли удалить их более точно. «Многие фармацевтические компании сейчас ищут небольшие белки с медицинским потенциалом», — говорит биохимик Гленн Кинг из Университета Квинсленда в Сент-Люсии, Австралия. «Это одно из самых быстрорастущих направлений.«
Другие короткие аминокислотные цепи, часто называемые пептидами или полипептидами, изобилуют клетками, но они представляют собой урезанные остатки более крупных предшественников. Миорегулин и его миниатюрные собратья, напротив, рождаются маленькими. Насколько они могут быть крошечными, остается неясным. Как отмечает специалист по геномике микробов Ами Бхатт из Стэнфордского университета в Пало-Альто, Калифорния, плодовые мушки полагаются на микропротеин с 11 аминокислотами для роста нормальных ног, а некоторые микробы могут вырабатывать белки длиной менее 10 аминокислот.Но даже самые большие маленькие белки не соответствуют белкам среднего размера, таким как альфа-амилаза, фермент из 496 аминокислот в нашей слюне, который расщепляет крахмал.
До недавнего времени было обнаружено лишь несколько небольших белков из-за критерия идентификации генов, установленного около 20 лет назад. Когда ученые анализируют геном организма, они часто сканируют открытые рамки считывания (ORF), которые представляют собой последовательности ДНК, разграниченные сигналами, которые сообщают рибосомам клетки, ее линиям сборки белка, где начать и где остановиться.Отчасти для того, чтобы избежать большого количества данных, прошлые исследователи обычно исключали любую открытую рамку считывания, которая могла бы давать белок, содержащий менее 100 аминокислот у эукариот или 50 аминокислот у бактерий. Например, в дрожжах этот порог ограничивал список ORF примерно до 6000.
Ослабление этого критерия показывает, что клетки несут значительно больше ORF. Ранее в этом году постдок из Стэнфорда Хила Сберро Ливнат, Бхатт и его коллеги исследовали фрагменты генома микробов, населяющих четыре части человеческого тела, включая кишечник и кожу.Путем поиска небольших ORF, которые могут кодировать белки длиной от пяти до 50 аминокислот, исследователи идентифицировали около 4000 семейств потенциальных микробелков. Почти половина из них не похожи на известные белки, но последовательность для одной маленькой ORF предполагает, что соответствующий белок находится в рибосомах — это намек на то, что он может играть фундаментальную роль. «Не только гены с эзотерическими функциями были упущены из виду», когда ученые упускали из виду небольшие ОРС, — говорит Бхатт. «Это гены с ключевыми функциями.«
Впервые мы собираемся исследовать эту вселенную новых белков.
Джонатан Вайсман, Калифорнийский университет, Сан-Франциско
Другие клетки также содержат огромное количество коротких открытых рамок считывания — например, дрожжи могут производить более 260 000 молекул, содержащих от двух до 99 аминокислот. Но клетки почти наверняка не используют все эти открытые рамки считывания, и некоторые из производимых ими аминокислотных цепочек могут не работать. В 2011 году, обнаружив более 600000 коротких ORF в геноме плодовой мухи, генетик по вопросам развития Хуан Пабло Кузо из Университета Сассекса в Брайтоне, США.К. и его коллеги пытались сократить число. Они рассудили, что, если конкретная ORF имеет идентичную или почти идентичную копию у родственного вида, вероятность того, что это геномный мусор, меньше. После поиска генома другой плодовой мушки и анализа других доказательств того, что последовательности транслируются, группа в конечном итоге получила более управляемую цифру в 401 короткую ORF, которая может давать микробелки. Это все равно составляет значительную часть белкового репертуара насекомых — они содержат около 22 000 полноразмерных белков.
Вайсман и его коллеги обнаружили микробелки вторым путем, с помощью метода, который они изобрели, чтобы в целом определить, какие белки производят клетки. Чтобы создать любой белок, клетка сначала копирует ген в информационную РНК. Затем рибосомы считывают мРНК и соединяют аминокислоты в указанном порядке. Посредством секвенирования мРНК, прикрепленных к рибосомам, Вайсман и его команда точно определяют, какие клетки фактически превращаются в белки, а где на РНК рибосома начинает считываться. В исследовании Cell 2011 года он и его команда применили этот метод профилирования рибосом, также называемый Ribo-seq, к эмбриональным стволовым клеткам мыши и обнаружили, что клетки вырабатывают тысячи неожиданных белков, в том числе многие из них, уровень которых ниже 100 аминокислот. — отсечка кислоты.«Было совершенно ясно, что стандартное понимание игнорировало большую вселенную белков, многие из которых были короткими», — говорит Вайсман.
Сагательян и его коллеги применили третий подход, чтобы обнаружить кладезь микробелков в наших собственных клетках. Исследователи использовали масс-спектрометрию, которая включает разбиение белков на части, которые сортируются по массе, чтобы получить отличительный спектр для каждого белка. Сагателян, его тогдашний постдок Сара Славофф и коллеги применили этот метод к смесям белков из человеческих клеток, а затем вычли сигнатуры известных белков.Этот подход позволил выявить спектры 86 ранее не обнаруженных крошечных белков, самые маленькие из которых имеют длину всего 18 аминокислот, сообщили исследователи в 2013 году в журнале Nature Chemical Biology .
Малый размер ограничивает возможности белка. Более крупные белки складываются в сложные формы, подходящие для определенной функции, например, для катализирования химических реакций. По словам химика Хулио Камареро из Университета Южной Калифорнии в Лос-Анджелесе, белки с размером меньше 50-60 аминокислот, вероятно, не складываются.Так что они, вероятно, не подходят в качестве ферментов или структурных белков.
Однако их миниатюрный размер также открывает новые возможности. «Они достаточно крошечные, чтобы поместиться в укромных уголках и трещинах более крупных белков, которые функционируют как каналы и рецепторы», — говорит Олсон. Маленькие белки часто разделяют короткие отрезки аминокислот со своими более крупными партнерами и, следовательно, могут связываться с этими белками и изменять их активность. Связанные микробелки также могут переносить более крупные молекулы в новые места, например, помогая им проникать в клеточные мембраны.
Микропротеин в яде скорпиона-ловца смерти был слит с флуоресцентным красителем, чтобы опухоли испускали свет в ближнем инфракрасном диапазоне. ( 1 ) Опухоль в видимом свете ( 2 ) Та же опухоль в видимом и ближнем инфракрасном свете
(Сверху вниз) ИВАН КУЗЬМИН / НАУЧНЫЙ ИСТОЧНИК; BLAZE BIOSCIENCE (2)Из-за их притяжения к более крупным белкам маленькие белки могут дать клеткам обратимый способ включать или выключать более крупные белки.В исследовании 2016 года, проведенном в PLOS Genetics , биолог по развитию растений Стефан Венкель из Копенгагенского университета и его коллеги генетически изменили растений Arabidopsis для производства дополнительных количеств двух небольших белков. Обычно растения зацветают, когда дни достаточно длинные, но когда они производят избыточное количество двух микробелков, их цветение откладывается. Маленькие белки вызвали эту задержку, блокируя здоровенный белок CONSTANS, который запускает цветение. Они привязывают CONSTANS к другим ингибирующим белкам, которые его отключают.«Клетка использует то, что помогает ей выжить. Если короткий белок выполняет свою работу, это нормально», — говорит Сагателян.
Эти задания включают в себя другие ключевые задачи. В 2016 году Славофф, Сагателян и его коллеги обнаружили, что человеческие клетки производят 68-аминокислотный белок, который они назвали NoBody, который может помочь управлять разрушением неисправных или ненужных молекул мРНК. Название NoBody отражает его роль в предотвращении образования процессинговых телец (P-телец), загадочных кластеров в цитоплазме, где может происходить распад РНК.Когда белок отсутствует, образуется больше Р-телец, что ускоряет разрушение РНК и изменяет внутреннюю структуру клетки. «Это показывает, что небольшие белки могут оказывать огромное влияние на клетку», — говорит Славофф.
Мышцы зависят от множества микробелков. Во время эмбрионального развития отдельные мышечные клетки сливаются в волокна, обеспечивающие сокращение. Миомиксер из 84 аминокислотных белков объединяется с более крупным белком, чтобы объединить клетки, сообщила команда Олсона в 2017 году в Science .Без него эмбриональные мыши не могут формировать мышцы и почти прозрачны.
Позже миорегулин начинает регулировать мышечную активность. Когда мышца получает стимул, клетки-хранилища высыпают кальций, заставляя волокна сокращаться и генерировать силу. Затем ионный насос SERCA начинает возвращать кальций в запасы, позволяя мышечным волокнам расслабиться. Команда Олсона обнаружила, что миорегулин связывается с SERCA и ингибирует его. Эффект ограничивает частоту сокращения мускулов мыши — возможно, гарантируя, что у животного есть резерв мышечной силы на случай чрезвычайной ситуации, например, при побеге от хищника.Другой небольшой белок, DWORF, имеет противоположный эффект, высвобождая SERCA и позволяя мышце многократно сокращаться.
Даже широко изученные организмы, такие как кишечная бактерия Escherichia coli , содержат неожиданные маленькие белки, которые выполняют важные функции. В 2012 году Сторц и ее команда сообщили, что ранее неизвестный белок из 49 аминокислот под названием AcrZ помогает микробу выжить при некоторых антибиотиках, стимулируя насос, который выталкивает лекарства.
А яд, производимый множеством организмов, включая пауков, многоножек, скорпионов и ядовитых моллюсков, изобилует крошечными белками.Многие компоненты яда выводят из строя или убивают, блокируя каналы для натрия или других ионов, которые необходимы для передачи нервных импульсов. Маленькие белки «поражают эти ионные каналы с удивительной специфичностью и эффективностью», — говорит Кинг. «Они являются основными компонентами ядов и ответственны за большинство фармакологических и биологических эффектов».
Австралийский гигантский водяной клоп, убивающий рыбу, например, полагается не только на острые когти и похожие на копья рты, чтобы подчинить себе добычу. Он вводит своим жертвам смесь из более чем 130 белков, 15 из которых содержат менее 100 аминокислот, сообщили Кинг и его коллеги в прошлом году.
В отличие от гигантских белков, таких как антитела, микропротеины, доставляемые с помощью таблеток или инъекций, могут проникать в клетки и изменять их функции. Каптоприл, первый из класса лекарств от высокого кровяного давления, известных как ингибиторы ангиотензинпревращающего фермента, был разработан из небольшого белка в яде бразильской гадюки. Но лекарство, которое Управление по санитарному надзору за качеством пищевых продуктов и медикаментов одобрило для продажи в Соединенных Штатах в 1981 году, было обнаружено случайно, еще до того, как ученые выделили небольшие белки в отдельную группу.На данный момент только несколько микробелков вышли на рынок или в клинические испытания.
Исследователи рака пытаются извлечь выгоду из микробелка из яда скорпиона-ловца смерти ( Leiurus quinquestriatus ) из Африки и Ближнего Востока. Молекула имеет загадочное притяжение к опухолям. Объединив его с флуоресцентным красителем, ученые надеются осветить границы опухолей головного мозга, чтобы хирурги могли безопасно вырезать раковые ткани. «Он освещает опухоль. Вы можете видеть края и метастазы», - говорит Кинг.В настоящее время проводится клиническое исследование, посвященное оценке того, может ли двойная молекула помочь хирургам удалять опухоли головного мозга у детей.
Насколько важны малые белки для медицины, пока неизвестно, но они уже опровергли несколько биологических предположений. Генетик Норберт Хюбнер из Центра молекулярной медицины Макса Дельбрюка в Берлине и его коллеги обнаружили десятки новых микробелков в клетках сердца человека. Группа проследила их до неожиданного источника: короткие последовательности в длинных некодирующих РНК, разновидность, которая, как считалось, не продуцирует белки.После идентификации 169 длинных некодирующих РНК, которые, вероятно, считывались рибосомами, Хюбнер и его команда использовали тип масс-спектрометрии, чтобы подтвердить, что более половины из них дают микробелки в клетках сердца, результат был сообщен ранее в этом году в Cell .
Бактерии, такие как Escherichia coli , также производят множество микробелков, хотя их функции во многих случаях остаются неясными.
КВАНШИН КИМ / НАУЧНЫЙ ИСТОЧНИКПоследовательности ДНК других крошечных белков также встречаются в нетрадиционных местах.Например, некоторые из них находятся рядом с открытыми рамками считывания для более крупных белков. Ранее исследователи думали, что эти последовательности помогают управлять производством более крупных белков, но редко дают начало самим белкам. Некоторые кодирующие последовательности для недавно открытых микробелков даже вложены в последовательности, кодирующие другие, более длинные белки.
Эти геномные сюрпризы могут пролить свет на то, как возникают новые гены, говорит биолог-эволюционист Анн-Руксандра Карвунис из Университета Питтсбурга в Пенсильвании.Исследователи думали, что большинство новых генов возникает, когда существующие гены дублируются или сливаются, или когда виды обмениваются ДНК. Но для Карвуниса микробелки предполагают, что протогены могут образовываться, когда мутации создают новые сигналы запуска и остановки в некодирующей части генома. Если полученная в результате ORF продуцирует полезный белок, новые последовательности останутся в геноме и будут подвергаться естественному отбору, в конечном итоге превратившись в более крупные гены, которые кодируют более сложные белки.
В исследовании 2012 года Карвунис, который тогда был постдоком в лаборатории Марка Видаля в Институте рака Дана-Фарбер в Бостоне, и его коллеги обнаружили, что дрожжи транслируют более 1000 коротких ORF в белки, подразумевая, что эти последовательности являются протогенами.В новом исследовании Карвунис и ее команда проверили, могут ли молодые ORF быть полезными для клеток. Они генетически изменили дрожжи, чтобы увеличить выход 285 недавно разработанных ORF, большинство из которых кодируют молекулы, которые меньше стандартного порогового значения белка или чуть выше него. Для почти 10% белков увеличение их уровней усиливало рост клеток по крайней мере в одной среде. Результаты, опубликованные на сервере препринтов bioRxiv, предполагают, что эти последовательности могут стать полноценными генами, говорит Карвунис.
Славофф до сих пор вспоминает, как был поражен, когда во время интервью на постдока с Сагателяном он спросил, не захочет ли она пойти на охоту за маленькими белками. «Я никогда не думал, что может существовать такой размер белков, который до сих пор был для нас темным».
Но ставка окупилась — теперь у нее есть собственная лаборатория по поиску микробелков. Недавно она рассказала некоторым из своих постдоков и аспирантов об одном из наиболее изученных организмов, штамме K12 E.coli. Вскоре команда обнаружила пять новых микробелков. «Мы, вероятно, только царапаем поверхность», — говорит она.
Biology4Kids.com: Структура клетки: Рибосомы
Клеткам необходимо производить белков . Белковые ферменты ускоряют биологические процессы. Другие белки поддерживают клеточные функции и находятся в мембранах. Белки даже составляют большую часть ваших волос. Когда клетке нужно производить белки, она ищет рибосомы. Рибосомы являются строителями белка или синтезаторами белка клетки. Они похожи на строителей, которые соединяют по одной аминокислоте за раз и выстраивают длинные цепочки.
Рибосомы особенные, потому что они встречаются как у прокариот, так и у эукариот. Хотя такая структура, как ядро, встречается только у эукариот, каждой клетке необходимы рибосомы для производства белков. Поскольку у прокариот нет мембраносвязанных органелл, рибосомы свободно плавают в цитозоле.
Рибосомы встречаются во многих местах эукариотической клетки. Вы можете обнаружить их плавающими в цитозоле. Эти плавающие рибосомы производят белки, которые будут использоваться внутри клетки. Другие рибосомы находятся в эндоплазматической сети. Эндоплазматический ретикулум с прикрепленными рибосомами называется грубым ER. Под микроскопом он выглядит ухабистым. Присоединенные рибосомы образуют белки, которые будут использоваться внутри клетки, и белки, предназначенные для экспорта из клетки. К ядерной оболочке также прикреплены рибосомы.Эти рибосомы синтезируют белки, которые попадают в перинуклеарное пространство.
Каждая рибосома состоит из двух частей или субъединиц. У эукариот ученые идентифицировали субъединицы 60-S (большие) и 40-S (маленькие). Несмотря на то, что рибосомы имеют немного разные структуры у разных видов, их функциональные области очень похожи.Например, у прокариот рибосомы немного меньше, чем у эукариот. Модель 60-S / 40-S отлично подходит для эукариотических клеток, в то время как прокариотические клетки имеют рибосомы, состоящие из 50-S и 30-S субъединиц.Это небольшая разница, но одна из многих, которые вы найдете в двух разных типах ячеек. Ученые использовали это различие в структуре рибосом для разработки лекарств, которые могут убивать прокариотические микроорганизмы, вызывающие заболевания. Существуют даже структурные различия между рибосомами, обнаруженными в митохондриях, и свободными рибосомами.
Когда рибосомы используются в процессе синтеза белка? Когда клетке необходимо производить белок, в ядре создается мРНК. мРНК затем отправляется из ядра в рибосомы.Когда приходит время производить белок, две субъединицы объединяются и соединяются с мРНК. Субъединицы фиксируются на мРНК и запускают синтез белка.
Процесс создания белков довольно прост. Во-первых, вам нужна аминокислота. Еще одна нуклеиновая кислота, которая живет в клетке, — это РНК переноса . тРНК связана с аминокислотами, плавающими вокруг клетки. С помощью инструкций по предложению мРНК рибосома соединяется с тРНК и извлекает одну аминокислоту. Затем тРНК высвобождается обратно в клетку и присоединяется к другой аминокислоте.Рибосома выстраивает длинную аминокислотную (полипептидную) цепь, которая в конечном итоге станет частью более крупного белка.
Клетки мозга из клеток кожи (видео Кембриджского университета)
Полезные справочные ссылки
Encyclopedia.com:http://www.encyclopedia.com/topic/Ribosomes.aspx
Википедия:
http://en.wikipedia.org/wiki/Ribosomes
Encyclopdia Britannica:
http: // www.britannica.com/EBchecked/topic/502164/ribosome
белков
Аминокислоты
Белки — самые разнообразные биомолекулы на Земле, выполняющие множество функций, необходимых для жизни. Белковые ферменты являются биологическими катализаторами, поддерживающими жизнь, регулируя, где и когда происходят клеточные реакции. Структурные белки обеспечивают внутреннюю и внешнюю поддержку для защиты и поддержания формы клеток. Например, кератины являются важным классом структурных белков, обнаруженных в волосах, коже, ногтях и перьях животных.Белки подвижности обеспечивают основу для движения клеток и всего организма, включая белки мышечных двигателей, которые могут перемещать целые животные! Мембранные белки передают сигналы во время межклеточной коммуникации, транспортируют молекулы в клетки и из них и защищают живые организмы, идентифицируя и помеча захватчиков.
Функции белков настолько разнообразны из-за множества уникальных трехмерных структур, которые образуют белковые полимеры. Несмотря на такое разнообразие, белки также имеют несколько общих структурных характеристик своих мономеров — аминокислот.Структурное сходство аминокислот делает синтез белка единообразным и регулируемым процессом; однако каждая аминокислота также содержит уникальный структурный компонент. Конкретные различия между каждой аминокислотой взаимодействуют, создавая уникальные трехмерные белковые структуры. В совокупности сходства и различия между аминокислотами объясняют, как клетки могут создавать разнообразный пул белков из одного и того же набора строительных блоков.
В каждой аминокислоте существует один центральный атом углерода — альфа-углерод (альфа-углерод).Из четырех групп атомов, ковалентно связанных с α-углеродом, три одинаковы для всех аминокислот. -Углерод всегда напрямую связан с одной аминогруппой и одной карбоксильной группой (карбоновой кислотой). Название аминокислота происходит от наличия этих двух функциональных групп (аминокислота + кислота). Все аминокислоты имеют третью общую ковалентную связь с атомом водорода, но четвертый атом (или атомная группа), связанный с α-углеродом, уникален в каждой аминокислоте.
Четвертая α-углеродная связь может соединяться с другим одиночным атомом водорода, как в глицине, или с группой атомов.Группы атомов различаются как по размеру, так и по полярности или заряду. Например, лизин содержит большую ионную группу атомов. Для простоты, когда конкретная аминокислота не идентифицирована, биологи используют термин «R-группа» для обозначения четвертого атома или группы, связанной с α-углеродом. Термин «R» обозначает остальную часть молекулы и используется при обсуждении общей структуры и реакционной способности аминокислот без усложнения структуры включением деталей R-группы.
Синтез белка включает построение полимера из аминокислот со сложной трехмерной структурой.Синтез дегидратации образует пептидную связь между аминокислотами и высвобождает молекулу воды. Дипептид образуется, когда между двумя отдельными аминокислотами создается пептидная связь, соединяющая углерод карбоксильной группы одной аминокислоты и азот аминогруппы другой аминокислоты. Поскольку дополнительные аминокислоты связываются посредством синтеза дегидратации, короткая цепь (пептид) растет. Полипептиды образуются, когда длина пептидной цепи достигает ста или более аминокислот. Белки образуются в виде аминокислот в одном или нескольких полипептидах, химически взаимодействуя с образованием сложной трехмерной структуры.
Живые организмы синтезируют почти все белки, используя всего двадцать различных аминокислот. Полипептиды образуют уникальную трехмерную структуру, основанную на типе и положении (последовательности) этих аминокислот. Внутри последовательности R-группы аминокислот образуют химические взаимодействия, которые создают определенную трехмерную структуру. Эти R-группы обычно называют «боковыми цепями», потому что они не участвуют в пептидных связях. R-группы выступают на стороне полипептида, позволяя им химически взаимодействовать друг с другом.Взаимодействие с боковыми цепями формирует специфическую структуру каждого белка, структуру, уникально способную выполнять клеточную функцию этого белка.
Функциональные группы белков
Это задание проверяет вашу способность определять функциональные группы аминокислот в белках.
Построение и расщепление белков
Это задание проверяет вашу способность идентифицировать реагенты и продукты синтеза и гидролиза белка.
Структура и функции белка
В отличие от полисахаридов, полипептидные цепи собраны с широким спектром аминокислот в каждом полимере.Набор из двадцати аминокислот, обычно содержащихся в биологических белках, напрямую отвечает за разнообразие белковых структур в живых клетках. Каждый белок отличается по нескольким аспектам, которые определяют структуру и, следовательно, функцию. Белок может состоять из одной или нескольких полипептидных цепей. Гены клетки определяют длину каждой полипептидной цепи, а также тип и положение каждой аминокислоты в последовательности. Вместе эти факторы определяют структуру белка, которая определяет функцию, которую может выполнять белок.
Как структура белка определяет функцию? Трехмерная форма каждого белка идеально подходит для выполнения одной конкретной функции. Например, аквапорины — это канальные белки, которые образуют небольшие туннели через клеточную мембрану. Внутренняя поверхность аквапориновых туннелей имеет определенный диаметр и полярность. Эта структура идеально подходит для переноса молекул воды, но очень немногого другого, обеспечивая специфичность и функцию. Если структура белка изменяется, меняется и его способность функционировать.
Зная важность структуры белка в определении функции, как тогда определяется структура белка? Чтобы ответить на этот вопрос, мы должны сначала спросить, как только двадцать аминокислот могут создать разнообразие белков, которые мы видим в живых организмах. Это разнообразие легко объяснить тем, как полипептиды образуют последовательность. Представьте себе создание дипептида с использованием двадцати распространенных аминокислот. Существует двадцать вариантов для первого положения и двадцать вариантов для второго положения этого двух аминокислотного пептида.Математические расчеты говорят нам, что мы могли синтезировать четыреста различных дипептидов! Для каждых дополнительных аминокислот в пептиде мы снова умножаем это количество вариантов на двадцать. Представьте себе, сколько различных полипептидов может существовать в природе, имея более ста аминокислот в средней последовательности!
Помимо увеличения вариативности, каждая из двадцати общих аминокислот играет жизненно важную роль в структуре и функции белков во всех живых организмах. В то время как производители, такие как растения, синтезируют все двадцать распространенных аминокислот, потребители, которые получают энергию, поедая биомолекулы, полагаются на потребление с пищей для получения одной или нескольких аминокислот.Люди синтезируют десять из двадцати обычных аминокислот, но оставшиеся десять должны быть получены с пищей. Хотя всех аминокислот необходимы для жизни человека, «незаменимые аминокислоты» — это те, которые человек не может синтезировать самостоятельно. Употребление в пищу продуктов, богатых белком, обеспечивает клетки этими незаменимыми аминокислотами.
Живые организмы, управляемые генами, синтезируют полипептиды с использованием аминокислот. Уникальный порядок аминокислот в полипептиде называется первичной структурой и представляет собой первый уровень трехмерной структуры (конформации) белка.Первичная структура определяет каждый дополнительный уровень химических взаимодействий, управляя формированием окончательной конформации белка.
Если структура определяет функцию, как первичная последовательность аминокислот определяет трехмерную структуру? В процессе, называемом сворачиванием белка, стабильные химические взаимодействия образуются между аминокислотами в белке, изгибая и скручивая полимер в трехмерную форму. Сворачивание белков иногда требует помощи молекулярных белков-шаперонов, которые связывают вновь образующиеся полипептиды и способствуют формированию структуры.
Сворачивание белка включает три уровня химических взаимодействий, называемых вторичной, третичной и четвертичной структурой. Вторичная структура создается за счет образования водородных связей между соседними аминокислотами во время синтеза белка. Водородные связи во вторичной структуре включают полярные амино- и карбоксильные группы аминокислот, но не включают R-группы. По мере того как пептидная цепь продолжает расти, взаимодействия между боковыми цепями аминокислот (R-группами) образуют третичную структуру полипептида.Боковые цепи взаимодействуют друг с другом посредством:
- образование водородных связей в боковой цепи.
- агрегация гидрофобных боковых цепей.
- образование ионных (солевой мостик) и ковалентных (дисульфидный мостик) связей.
Хотя все химические взаимодействия важны для третичной структуры, белки сворачиваются в основном в ответ на то, какие боковые цепи способны образовывать водородные связи с водой. Поскольку молекулы воды составляют большую часть внутреннего раствора клетки, неполярные боковые цепи исключаются из раствора и объединяются по мере образования водородных связей с полярными и ионными боковыми цепями.Эти гидрофобные взаимодействия являются сильнейшим фактором, определяющим третичную структуру.
У некоторых белков сворачивание завершается после образования третичной структуры. В других случаях несколько полипептидных цепей объединяются, образуя четвертый уровень структуры, четвертичную структуру. Четвертичная структура включает два или более полипептидов, складывающихся вместе посредством тех же типов химических взаимодействий, которые сформировали третичную структуру. В четвертичной структуре боковые цепи разных полипептидов образуют водородные связи, гидрофобные взаимодействия и химические связи друг с другом.Гемоглобин, белок, переносящий кислород через кровоток, состоит из четырех полипептидов.
Что делать, если что-то нарушает структуру белка? Сильная жара, изменения pH и химические токсины — это лишь некоторые из причин денатурации белка, потери естественной структуры белка. Некоторые белки способны к рефолдингу, но большинство белков не могут восстановиться после значительной потери структуры белка. Например, приготовление яйца навсегда денатурирует его белки, изменяя внешний вид и текстуру яйца.Живые клетки затрачивают значительные усилия на поддержание гомеостаза, контролируя их внутреннюю среду, потому что неожиданные изменения могут разрушить белки клетки, убивая клетку.
Поскольку функция белка зависит от точного формирования структуры, сворачивание белка является ключевой темой научных исследований. Многие биохимики посвящают всю свою карьеру поиску способов предсказать, как будут складываться белки и как мутации повлияют на структуру и функцию белков. Мутации, которые изменяют первичную последовательность белка, могут привести к массивным изменениям в структуре белка и устранить или изменить функцию, что приведет к болезни или смерти.Иногда мутации приводят к улучшенным или новым функциям, приносящим пользу организму. Редкие полезные мутации распространяются среди популяций посредством естественного отбора, что приводит к эволюционным изменениям.
Денатурация белка
Эта анимация иллюстрирует процесс денатурации.
Белковые термины
Это задание проверяет вашу способность сопоставлять термины, относящиеся к белкам, с их определениями.
Роль белков
Белки
Роль белков
ср протеин нужен для роста и ремонта.Белки используются для производства клеток нашего тела. В частности, они используются при образовании новой протоплазмы. Антитела, ферменты и гормоны также состоят из белков. Наконец, белки могут обеспечить мы с энергией (хотя организм расщепляет белок только тогда, когда все углеводов и жиров нет: другими словами, когда вы голодаете).
Почему они называются белками?
Белка происходит от греческого слова proteios, что означает «первичный» или «занимающий первое место».»Голландский химик Джерард Иоганн Малдер придумал слово протеин в 1838 году.
Аминокислоты
Белки состоят из цепочек аминокислот. Есть двадцать различных аминокислот, поэтому клетке требуется много информации, чтобы белок вместе (, что из 20 это первая аминокислота в цепи, вторая, третья так далее). Эта информация в конечном итоге исходит от ДНК.Белок часто состоит сотен аминокислот, связанных вместе.
Еда Источники белков
худой мясо, рыба, яйца, молоко и сыр — важные источники животного белка. Все растения содержат белок, но бобы, орехи или злаки — лучшее растение источники.
Энергия белков
В отличие от углеводов или жиров, которые могут дать нам энергия, белки обычно используются для построения частей клетки.Другими словами они представляют собой сырье, необходимое клетке для производства клеток и тканей. Когда съедается избыток белка, лишний белок может быть разбит на энергоемкие соединения. Потому что белков намного меньше, чем углеводов и дает те же 4 калории на грамм, потребление мяса сверх нормы потребности организма в создании тканей становятся неэффективным способом производства энергия.
Полные и неполные белки
Завершено белки — это продукты, содержащие все необходимые аминокислоты.Большинство животных продукты, такие как мясо, птица, рыба, яйца, сыр и молоко, являются полноценными белки. Некоторые растительные белки тоже являются полноценными. Соевые продукты, такие как тофу, также являются полноценными белками. Яйца — хороший источник полноценных белков.
Неполные белки — это белки, содержащие небольшие количества одной или нескольких незаменимых аминокислот. Большинство растительных продуктов неполноценны, например: бобовые (фасоль и горох), орехи, семена, зерна и овощи.
Объединение неполных белков для получения полных белков
Хотя растительные белки неполноценны, еще можно получить все необходимое аминокислоты, употребляя в пищу комбинацию растительных белков.Например, арахис сливочное масло с низким содержанием метионина аминокислоты. Хлеб много метионина, но не хватает лизина и изолейцина. Так бутерброд с арахисовым маслом становится полноценным белок.
Продукты животного происхождения содержат полноценные белки потому что они включают в себя все незаменимые аминокислоты. В большинстве диет рекомендуется сочетание растительного и животного белка: 0,8 грамма на килограмм веса тела считается безопасной дневной нормой для нормального взрослого человека.
Белок связанные проблемы со здоровьем.
Слишком много белка в рационе может быть опасным. Дополнительный Белок содержит азот, который в печени превращается в отходы, называемые мочевиной. Почки выводят азотные отходы с мочой. Слишком много белка может положить нагрузка на печень и почки. Когда необходимо образовать лишнюю мочу для удаления избыток отходов, организм может обезвоживаться.Слишком много белка также может сделать один лишний вес, так как избыток белков в печени превращается в жиры, которые хранится в организме.
Недостаток белков приведет к ослаблению организма, неспособному бороться с болезнями. Диета может привести к тому, что организм не получит достаточно питательных веществ. Вы можете получить достаточно калорий для удовлетворения ваших энергетических потребностей, но у вас нет всех необходимых аминокислот. кислоты.
Недостаток белка практически неизвестен в рационе питания в этой стране (поэтому компании, продвигающие белка напитки или добавки с аминокислотами тратят ваши деньги ). Следующая записьКак уменьшить боль в пояснице: Ваша боль в спине — Ravijuhend |






 Аминокислоты, высвобождающиеся при расщеплении белковых молекул, используются для построения новых белков.
Аминокислоты, высвобождающиеся при расщеплении белковых молекул, используются для построения новых белков.
Добавить комментарий