Понижен эстрадиол: норма, высокие и низкие показатели количества эстрогенов
Анализ на эстрадиол в Колпино
Эстрадиол – это один из главных и наиболее активных женских половых гормонов. Он отвечает за половое созревание и развитие вторичных половых признаков у женщин. Понижение или повышение уровня гормона в организме может повлиять на общее самочувствие, способность женщины забеременеть, выносить ребенка.
Общая информация
Эстрадиол – это наиболее активный гормон в организме женщины. Он вместе с прогестероном регулирует репродуктивную функцию и отвечает за сохранение беременности.
Большая часть гормона синтезируется в яичниках, небольшое количество вырабатывается в коре надпочечников. Во время беременности вырабатывать эстрогены начинает плацента. У мужчин эстрогены вырабатываются в надпочечниках и яичках.
Показания к проведению исследования
Анализ может быть назначен при наличии следующих показаний:
- диагностика нарушений фертильности и менструального цикла у взрослых женщин;
- отсутствие овуляции;
- олигоменорея, аменорея;
- маточные кровотечения неясной этиологии;
- гипогонадизм;
- гирсутизм;
- остеопороз;
- нарушение полового созревания;
- выраженный предменструальный синдром;
- бесплодие;
- бактериальный вагиноз;
- оценка текущего состояния фетоплацентарного комплекса на ранних сроках беременности;
- признаки женственности у мужчин.

Результаты анализа
Пониженный уровень эстрадиола при повышенных показателях ЛГ и ФСГ может быть симптомом яичниковой недостаточности. Кроме этого, пониженный эстрадиол может быть при СПКЯ и во время менопаузы.
Повышенный уровень гормона может быть признаком беременности, заболеваний печени, а также симптомом образования опухоли, которая производит эстрогены. Чаще всего анализ на эстрадиол назначают совместно с анализами на другие гормоны (прогестерон, ЛГ, ФСГ).
В Колпино сделать анализ на эстрадиол вы можете в клинике «Мир здоровья».
Здоровья Вам!
Эстрадиол (S-E2) – SYNLAB Eesti
Эстрадиол – наиболее биологически активный стероидный гормон. Продуцируется в яичниках – теле фолликулов и клетках гранулярной части, а также в коре надпочечников и плаценте. Циркулирует в крови, большей частью, связанным с глобулином, связывающим половые гормоны (SHBG).
Эстрогены относятся к стимуляторам развития вторичных половых признаков у женщин и определяют развитие характерных для женщин физических и психических признаков. Также эстрадиол принимает участие в регуляции процесса минерализации костей.
Также эстрадиол принимает участие в регуляции процесса минерализации костей.
Секреция эстрадиола зависит от фазы менструального цикла. В фолликулярной фазе его концентрация увеличивается под действием гонадотропинов, достигая максимума перед овуляцией. Под действием эстрадиола в фазе созревания фолликула происходит пролиферация клеток эндометрия. После этого содержание эстрогенов уменьшается и увеличивается вновь вместе с концентрацией прогестерона в лютеальной фазе, ингибируя выделение гонадотропинов.
У детей и женщин в постменопаузе содержание эстрогенов очень низкое.
Показания:
У женщин:
- Оценка овариальной функции (примарная и секундарная аменорея и олигоаменоррея, бесплодие)
- Контроль медикаментозно стимулированной овуляции
- Выяснение причин раннего пубертета
- Контроль за лекарственной терапией эстрогенами
У мужчин:
- Гинекомастия, гипогонадизм
Метод анализа: Хемилюминисцентный метод
Референтные значения:
| < 1 г Ж | < 181 pmol/L |
| 1 – 5 л Ж | < 91 pmol/L |
| 6 – 10 л Ж | < 139 pmol/L |
| 11 – 14 л Ж | < 431 pmol/L |
> 14 л.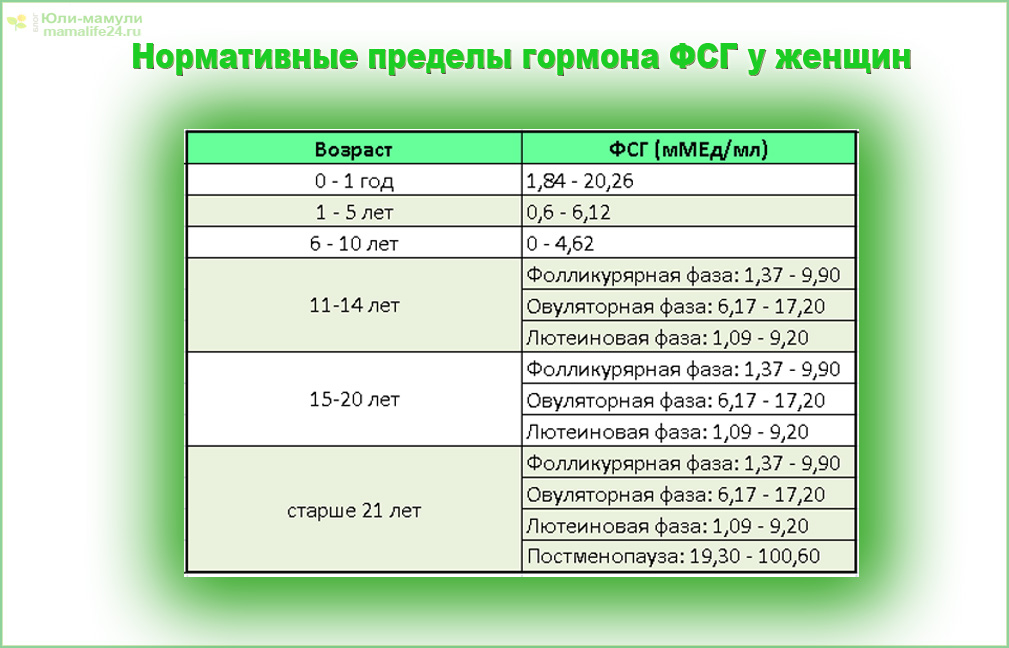 Фаза фолликула, Ж Фаза фолликула, Ж | 72 – 529 pmol/L |
| Фаза овуляции, Ж | 234 – 1309 pmol/L |
| Лютеиновая фаза, Ж | 205 – 786 pmol/L |
| Постменопауза, Ж | < 118 pmol/L |
| < 1 г M | < 79 pmol/L |
| 1 – 5 л M | < 97 pmol/L |
| 6 – 10 л M | < 75 pmol/L |
| 11 – 14 л M | < 100 pmol/L |
| > 14 л M | < 146 pmol/L |
Интерпретация результата:
Стероидные гормоны вместе с гонадотропинами (LH и FSH) очень важны в регуляции гипоталамо-гипофизарно-овариальной системы. Поскольку эстрадиол продуцируется, в основном, в яичниках, то его определение дает информацию о функции яичников и протекании овуляции. Во время овуляции значение Е2 должно повышаться.
Высокие значения E2 у женщин:
- Опухоль яичников – у женщин в постменопаузе
- Преждевременный пубертет
- Избыточный вес
Высокие значения E2 у мужчин:
- Гинекомастия
- Тератомы, а также опухоли надпочечников и яичек, вырабатывающие эстрогены
Низкие значения E2 у женщин:
- Обусловленная гипогонадизмом примарная и секундарная аменорея – ановуляторный цикл (низкие значения Е2 в фазе фолликула, фолликул не входит в преовуляторную фазу)
- Недостаточность желтого тела Corpus luteum.
 Значения эстрадиола в первой фазе низкие, отсутствует второй пик лютеиновой фазы
Значения эстрадиола в первой фазе низкие, отсутствует второй пик лютеиновой фазы
10 гормонов, которые влияют на нашу красоту
Наш организм – это сложная система, в которой все процессы взаимосвязаны и отлажены природой. Малейшие сбои в его работе отражаются на функционировании всей системы, в том числе и нашей внешности. Изначальные данные, такие как цвет волос и тип телосложения, записаны в ДНК-коде и не меняются в течение жизни, а то, насколько упругой выглядит наша кожа и стройным тело, во многом зависит от уровня гормонов. Главных гормонов, которые влияют на нашу красоту, десять. Мы решили выяснить, что именно делает каждый из них и как гормональный дисбаланс отражается на внешности.
Эстроген
Эстрогены – это целая группа женских половых гормонов, к которым относятся эстрон, эстриол и эстрадиол. Все они вырабатываются в яичниках, отвечают за формирование фигуры по женскому типу, развитие половых органов и регулируют менструальный цикл. «Если эстроген вырабатывается в нормальном количестве, он очень положительно влияет на внешний вид женщины, – рассказывает Ирина Вяткина, врач гинеколог-эндокринолог «Клиники Марины Рябус». – Этот гормон участвует в процессе обновления клеток всего организма, в том числе и кожи. Эстроген положительно влияет и на красоту волос: придает им блеск, сохраняет молодость и здоровье. Эстрогены поднимают настроение, располагают к флирту и кокетству, препятствуют отложению холестерина в стенках сосудов, заставляют блестеть глаза, разглаживают морщинки, делают кожу эластичной и упругой, тем самым делая женщину красивой. Кроме того, эстрогены поднимают настроение и располагают к флирту и кокетству – они способствует развитию влечения у женщин к лицам мужского пола. На фоне увеличения выработки эстрогенов улучшается координация движений и тем самым походка, меняется качество речи. Она становится более приятной для восприятия».
«Если эстроген вырабатывается в нормальном количестве, он очень положительно влияет на внешний вид женщины, – рассказывает Ирина Вяткина, врач гинеколог-эндокринолог «Клиники Марины Рябус». – Этот гормон участвует в процессе обновления клеток всего организма, в том числе и кожи. Эстроген положительно влияет и на красоту волос: придает им блеск, сохраняет молодость и здоровье. Эстрогены поднимают настроение, располагают к флирту и кокетству, препятствуют отложению холестерина в стенках сосудов, заставляют блестеть глаза, разглаживают морщинки, делают кожу эластичной и упругой, тем самым делая женщину красивой. Кроме того, эстрогены поднимают настроение и располагают к флирту и кокетству – они способствует развитию влечения у женщин к лицам мужского пола. На фоне увеличения выработки эстрогенов улучшается координация движений и тем самым походка, меняется качество речи. Она становится более приятной для восприятия».
Эстроген по праву считается главным женским гормоном красоты. Его дефицит сказывается не только на самочувствии, но и на внешности: волосы становятся тусклыми и могут расти в ненужных местах (например, на подбородке или груди), а кожа выглядит бледной и начинает рано увядать.
Бывают ситуации, когда уровень эстрогена у женщины повышен. Это сопровождается нарушением половой функции (пропадают месячные или овуляция), образованием жира именно на животе и бедрах, а также предменструальным синдромом.
Прогестерон
Основная задача прогестерона – это развитие яйцеклетки и ее размещение в матке, поэтому его часто называют гормоном беременности. У небеременных женщин прогестерон также присутствует и повышается во второй фазе менструального цикла, что, увы, негативно сказывается на внешности. «Прогестерон способствует задержке жидкости в организме, повышает проницаемость сосудистой стенки, кожа становится растяжимой, повышается выделение кожного сала и появляются угревые высыпания.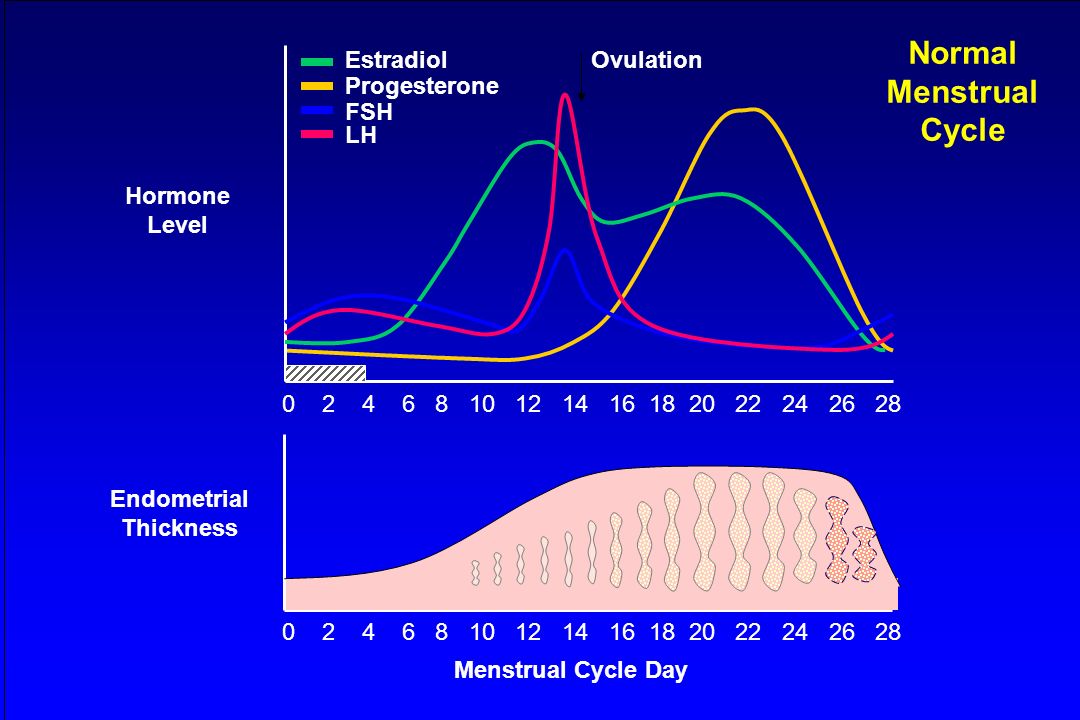
ДГЭА (дегидроэпиандростерон)
«ДГЭА – гормон, выделяемый надпочечниками. Он является предшественником половых гормонов, отвечает за половое влечение, ясный ум, твердую память, мышечную силу и физическую выносливость и улучшает настроение – все это является неотъемлемой частью молодости и красоты», – говорит Елена Шаткарь, эндокринолог резиденции красоты и долголетия GLMED. Пониженное содержание дегидроэпиандростерона негативно сказывается как на всем гормональном фоне, так и непосредственно на внешности и самочувствии.
Мелатонин
Мелатонин, известный как гормон сна, влияет и на многие другие функции организма. Он участвует в работе желудочно-кишечного тракта, эндокринной и иммунной систем, отвечает за нормальное функционирование клеток мозга и защиту от свободных радикалов. Да, мелатонин – это мощный антиоксидант, уровень которого влияет на то, как кожа и остальные органы могут самостоятельно противостоять свободным радикалам, разрушающим клетки. И это еще не все. «Действие мелатонина затрагивает сжигание жира во время сна, – рассказывает Елена Шаткарь. – Выработка гормона происходит во время сна в его наиболее глубокой фазе – примерно с 12 часов ночи до 4 часов утра. Главное существенное условие для его выработки – человек должен спать в темном помещении. Критерием темноты может служить факт невозможности рассмотреть свою вытянутую руку.
Кортизол
Мелатонин влияет на выработку кортизола – гормона стресса, который синтезируется надпочечниками и помогает выжить в экстренных ситуациях. «При изменении выработки кортизола меняются углеводный обмен и выработка инсулина, что приводит к изменению внешнего вида и качества кожи. При высоком уровне инсулина происходит нарушение работы сальных и потовых желез, кожа теряет свои естественные защитные свойства, легко поражается бактериальной и грибковой инфекцией, теряет свою упругость, эластичность, снижается синтез коллагена. При повышении уровня кортизола кожа истончается и становится склонной к появлению пигментации. При нормальной выработке кортизола кожа упругая, ровная и красивая», – рассказывает Ирина Вяткина. Повышенный кортизол способствует накоплению жира в области лица и живота, поэтому справедливо выражение, что стресс мешает похудеть.
При повышении уровня кортизола кожа истончается и становится склонной к появлению пигментации. При нормальной выработке кортизола кожа упругая, ровная и красивая», – рассказывает Ирина Вяткина. Повышенный кортизол способствует накоплению жира в области лица и живота, поэтому справедливо выражение, что стресс мешает похудеть.
Тестостерон
Тестостерон, хоть и считается условно мужским гормоном, у женщин также вырабатывается при помощи надпочечников и половых желез. Тестостерон имеет непосредственное влияние на красоту кожи. «Он повышает скорость обновления клеток эпидермиса и увеличивает выработку коллагена за счет стимуляции соединительной ткани, производящей протеины, необходимые для синтеза коллагена, – говорит Ирина Вяткина. – С возрастом наблюдается снижение синтеза тестостерона. В результате замедляется регенерация кожи, снижаются ее защитные функции и упругость». Такие же симптомы могут наблюдаться и в молодом возрасте из-за гормональных нарушений. Повышение уровня тестостерона в норме происходит во второй фазе цикла, что вместе с прогестероном провоцирует образование прыщей. Сейчас набирает популярность тестостероновая терапия, которая улучшает качество кожи при возрастном снижении синтеза гормона. Врачи предупреждают, что самостоятельным приемом тестостерона можно сильно навредить своему здоровью – такая терапия проводится только по показаниям под наблюдением эндокринолога.
Сейчас набирает популярность тестостероновая терапия, которая улучшает качество кожи при возрастном снижении синтеза гормона. Врачи предупреждают, что самостоятельным приемом тестостерона можно сильно навредить своему здоровью – такая терапия проводится только по показаниям под наблюдением эндокринолога.
Соматотропин
Соматотропин известен как гормон роста. Его влияние на красоту и молодость сложно переоценить. «Соматотропин отвечает за рост и восстановление костей, помогает нормализовать обменные процессы, усиливает сжигание жира и помогает печени вырабатывать энергию для всего организма, – рассказывает Елена Шаткарь. – С возрастом выработка гормона роста замедляется, в связи с этим начинаются процессы старения. Повысить уровень соматотропина помогают регулярные физические нагрузки, правильное питание и полноценный ночной сон». Выработка гормона роста начинает снижаться уже после 25 лет, а к 45 годам его синтез в два раза меньше, чем в детстве. Это сопровождается снижением качества сна, нарушением аппетита и увеличением массы тела.
Тиреотропный гормон, тироксин и трийодтиронин
Тиреотропный гормон, тироксин и трийодтиронин – это все гормоны щитовидной железы, которые работают сообща. Они участвуют практически во всех обменных процессах организма, регулируют метаболизм, скорость синтеза витаминов и поддерживают нормальную функцию дыхания. «При нехватке гормонов щитовидной железы (гипотиреозе) кожа становится сухой, ногти – ломкими, выпадают волосы. А при избытке гормонов щитовидной железы (гипертиреозе) кожа становится влажной, повышается потливость, а, несмотря на здоровый аппетит и достаточный прием пищи, человек теряет в весе. Однако сброшенные килограммы совсем не радуют, так как при этом серьезно нарушается работа сердца, – говорит Юрий Потешкин, к. м. н., врач-эндокринолог клиники «Атлас». – При первых симптомах, указывающих на неполадки с функционированием щитовидной железы, следует сделать анализ крови на тиреотропный гормон. Именно он регулирует функции тироксина и трийодтиронина и отражает их уровень в организме».
Комментарий косметолога
Юлия Щербатова, врач-дерматокосметолог, челюстно-лицевой хирург, главный врач «Клиники современной косметологии Юлии Щербатовой»:
«Любой гормональный дисбаланс – состояние, которое развивалось в организме долго, и его коррекция тоже займет какое-то, зачастую довольно продолжительное время. Все это время косметолог может и должен помогать пациенту решать проблемы, с которыми тот обратился. Мы ни в коем случае не должны ждать завершения лечения, чтобы заниматься косметологией. Работа в этом случае будет, скорее, симптоматическая. Если проблемы связаны с сосудистой сеткой, мы используем лазеротерапию, если пациент жалуется на акне – лечим акне, если его беспокоит пигмент – боремся с пигментом инъекциями и лазером. Словом, действуем по показаниям и состоянию.
Типологизировать проблемы с кожей и их связь с гормональными нарушениями вряд ли возможно, потому что они могут проявляться очень по-разному. Но совершенно точно могу сказать, что коррекция гормонального фона при участии грамотного эндокринолога сделает результат более выраженным и эффективным. А вот желание обойтись одной косметологией, без плановой терапии, – это, как правило, трата денег и времени на процедуры, которые не сработают или сработают недостаточно хорошо. И дело не в самих процедурах, а в патологиях пациента. Так, например, если убрать лазером сосудистую сетку с лица, но не решить проблемы с избытком эстрогена или дефицитом прогестерона, из-за которых она часто возникает, – сосуды быстро вернутся. То же касается и гиперпигментации: казалось бы, бесследно удаленные лазером пигментные пятна будут возвращаться до тех пор, пока не придут хотя бы в относительный порядок стероидные гормоны и гормоны гипофиза, влияющие на клетки-меланоциты. Словом, при эндокринных проблемах, которые сегодня бывают у большого количества пациентов, сочетание косметологии с плановой терапией работает на порядок лучше, чем что-то одно.»
А вот желание обойтись одной косметологией, без плановой терапии, – это, как правило, трата денег и времени на процедуры, которые не сработают или сработают недостаточно хорошо. И дело не в самих процедурах, а в патологиях пациента. Так, например, если убрать лазером сосудистую сетку с лица, но не решить проблемы с избытком эстрогена или дефицитом прогестерона, из-за которых она часто возникает, – сосуды быстро вернутся. То же касается и гиперпигментации: казалось бы, бесследно удаленные лазером пигментные пятна будут возвращаться до тех пор, пока не придут хотя бы в относительный порядок стероидные гормоны и гормоны гипофиза, влияющие на клетки-меланоциты. Словом, при эндокринных проблемах, которые сегодня бывают у большого количества пациентов, сочетание косметологии с плановой терапией работает на порядок лучше, чем что-то одно.»
Имейте в виду, что любая попытка самостоятельно исправить гормональный дисбаланс может повлечь за собой еще большие проблемы со здоровьем. Грамотный врач-эндокринолог может вам подобрать нужный тип и дозировку гормонозаместительной терапии. Порой можно обойтись и вовсе без нее: на нарушение работы гормональной системы может влиять любое другое заболевание и даже низкий уровень витаминов и микроэлементов. В таких случаях врач будет корректировать именно первопричину.
Порой можно обойтись и вовсе без нее: на нарушение работы гормональной системы может влиять любое другое заболевание и даже низкий уровень витаминов и микроэлементов. В таких случаях врач будет корректировать именно первопричину.
Сдать анализ на эстрадиол (E2, Estradiol)
Метод определения Твёрдофазный хемилюминесцентный иммуноанализ.
Исследуемый материал Сыворотка крови
Доступен выезд на дом
Онлайн-регистрацияСинонимы: Эстрадиол, Estradiol, 17-beta-estradiol, E2.
Краткая характеристика определяемого вещества Эстрадиол
Наиболее активный эстрогенный (женский) половой стероидный гормон.
У женщин вырабатывается в яичниках, в плаценте и в сетчатой зоне коры надпочечников под влиянием фолликулостимулирующего гормона (ФСГ), лютеинизирующего гормона (ЛГ) и пролактина. В небольших количествах эстрадиол образуется в ходе периферического преобразования тестостерона. У мужчин эстрадиол образуется в семенниках, в коре надпочечников, но большая часть – в периферических тканях за счёт преобразования тестостерона.
У женщин эстрадиол обеспечивает формирование половой системы по женскому типу, развитие женских вторичных половых признаков в пубертатном периоде, становление и регуляцию менструальной функции, развитие яйцеклетки, рост и развитие матки в течение беременности; отвечает за психофизиологические особенности полового поведения. Обеспечивает формирование подкожной жировой клетчатки по женскому типу. Снижая сопротивление сосудов матки, повышает в ней кровоток и стимулирует гиперплазию эндометрия. Овуляция наступает через 24-36 часов после возникновения надпорогового уровня эстрадиола. Необходимым условием осуществления эффектов эстрадиола является правильное соотношение с уровнем тестостерона. Эстрадиол обладает анаболическим действием, усиливает обмен костной ткани и ускоряет созревание костей скелета. Способствует задержке натрия и воды в организме. Снижает уровень холестерина и повышает свёртывающую активность крови. Эстрадиол влияет на выделение нейротрансмиттеров, способствуя повышению нервного напряжения, раздражительности.
Необходимым условием осуществления эффектов эстрадиола является правильное соотношение с уровнем тестостерона. Эстрадиол обладает анаболическим действием, усиливает обмен костной ткани и ускоряет созревание костей скелета. Способствует задержке натрия и воды в организме. Снижает уровень холестерина и повышает свёртывающую активность крови. Эстрадиол влияет на выделение нейротрансмиттеров, способствуя повышению нервного напряжения, раздражительности.
С какой целью определяют уровень Эстрадиола в крови
Определение уровня эстрадиола применяют для оценки функции яичников при нарушениях менструального цикла у женщин, а также при женском и мужском бесплодии, для выявления нарушений метаболизма стероидов, контроля гормональной терапии. Также возможно использовать этот тест в диагностике опухолей, вырабатывающих эстрогены, и при подозрении на нарушения метаболизма стероидов.
Что может повлиять на результат теста «Эстрадиол»
Суточные колебания концентрации эстрадиола в сыворотке связаны с ритмом секреции ЛГ (лютеинизирующего гормона): максимум приходится на период с 15 до 18 часов, а минимум – между 24 и 2 часами.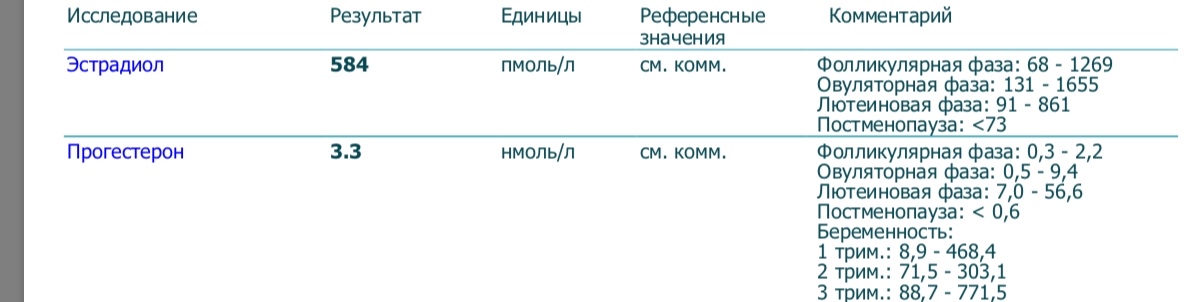 У мужчин уровень эстрадиола прогрессивно увеличивается, у мальчиков увеличение происходит в меньшей степени. У женщин детородного возраста уровень эстрадиола в сыворотке крови и плазме зависит от фазы менструального цикла. В начале цикла концентрация эстрадиола медленно возрастает. Наиболее высокий уровень эстрадиола отмечается в позднюю фолликулярную фазу. После овуляции уровень гормона снижается, возникает второй, меньший по амплитуде, подъём. Затем наступает спад концентрации гормона, продолжающийся до конца лютеиновой фазы. Во время беременности концентрация эстрадиола в сыворотке и плазме нарастает к моменту родов, а после родов она возвращается к норме на четвертый день. С возрастом у женщин наблюдается снижение концентрации эстрадиола. В постменопаузу концентрация эстрадиола снижается до уровня, наблюдаемого у мужчин.
У мужчин уровень эстрадиола прогрессивно увеличивается, у мальчиков увеличение происходит в меньшей степени. У женщин детородного возраста уровень эстрадиола в сыворотке крови и плазме зависит от фазы менструального цикла. В начале цикла концентрация эстрадиола медленно возрастает. Наиболее высокий уровень эстрадиола отмечается в позднюю фолликулярную фазу. После овуляции уровень гормона снижается, возникает второй, меньший по амплитуде, подъём. Затем наступает спад концентрации гормона, продолжающийся до конца лютеиновой фазы. Во время беременности концентрация эстрадиола в сыворотке и плазме нарастает к моменту родов, а после родов она возвращается к норме на четвертый день. С возрастом у женщин наблюдается снижение концентрации эстрадиола. В постменопаузу концентрация эстрадиола снижается до уровня, наблюдаемого у мужчин.
Пределы определения: 37,0 — 40370 пмоль/л.
Ассоциации половых гормонов с компонентами инсулин-глюкозного гомеостаза | Цыганкова
Введение
Известно, что нарушения углеводного обмена отчетливо демонстрируют гендерную специфику. У женщин они встречаются чаще, имеют более тяжелое течение и неблагоприятный прогноз. Особое внимание в этой связи привлекают специфичные для пола аспекты патогенетических изменений в системе ожирение-инсулин-глюкоза, обусловленные влиянием половых гормонов. Долгое время общепринятой являлась позиция, согласно которой эстрогены у женщин обладают протективным действием, а андрогены – негативным [1]. С другой стороны, накапливаются данные, что эстрогены как у женщин, так и у мужчин могут оказывать не только положительное, но и отрицательное влияние на метаболические параметры [1].
У женщин они встречаются чаще, имеют более тяжелое течение и неблагоприятный прогноз. Особое внимание в этой связи привлекают специфичные для пола аспекты патогенетических изменений в системе ожирение-инсулин-глюкоза, обусловленные влиянием половых гормонов. Долгое время общепринятой являлась позиция, согласно которой эстрогены у женщин обладают протективным действием, а андрогены – негативным [1]. С другой стороны, накапливаются данные, что эстрогены как у женщин, так и у мужчин могут оказывать не только положительное, но и отрицательное влияние на метаболические параметры [1].
Негативная роль высоких концентраций эндогенных андрогенов у женщин как модуляторов течения нарушений углеводного обмена до сегодняшнего дня окончательно не определена и в основном ограничивается изучением когорты пациенток с синдромом поликистозных яичников. Данные о положительной ассоциации дефицита тестостерона у мужчин как патогенетического фактора висцерального ожирения, дисбаланса проатерогенных цитокинов, лептинорезистентности и гипергликемии отмечаются в подавляющем большинстве публикаций, однако научные дебаты обусловлены различным пониманием причинно-следственных изменений уровней андрогенов, эстрогенов и компонентов инсулин-глюкозного гомеостаза [2, 3, 4]. Таким образом, несмотря на большой исследовательский материал, посвященный роли половых гормонов у пациентов с изменениями метаболизма инсулина, в настоящее время сохраняется много неизученных вопросов, неопределенных результатов, требующих детализации.
Таким образом, несмотря на большой исследовательский материал, посвященный роли половых гормонов у пациентов с изменениями метаболизма инсулина, в настоящее время сохраняется много неизученных вопросов, неопределенных результатов, требующих детализации.
Мужские половые стероиды и инсулинорезистентность
Инсулин и андрогены находятся в сложных взаимозависимых отношениях: как инсулин регулирует синтез и действие андрогенов, так и андрогены влияют на секрецию инсулина и чувствительность к нему. Классическое массачусетское исследование, в котором на протяжении 10 лет изучались процессы старения мужчин, показало, что у мужчин с низким уровнем тестостерона (Т) повышается риск развития инсулинорезистентности (ИР) и сахарного диабета 2 типа (СД2). Позже эти данные были неоднократно подтверждены другими авторами [5, 6]. Увеличивающееся количество наблюдений о протективном влиянии эндогенных андрогенов на чувствительность к инсулину у мужчин некоторые исследователи объясняют их трансформацией в эстрогены, однако D. Liu и соавт. (2008) показали, что эффект дегидроэпиандростерона сохранялся в присутствии ингибиторов эстрогеновых рецепторов [2]. M. Bekaert и соавт. (2015) также считают, что влияние Т – самостоятельный процесс и не зависит от активности ароматазы и баланса эстрогенов [3].
Liu и соавт. (2008) показали, что эффект дегидроэпиандростерона сохранялся в присутствии ингибиторов эстрогеновых рецепторов [2]. M. Bekaert и соавт. (2015) также считают, что влияние Т – самостоятельный процесс и не зависит от активности ароматазы и баланса эстрогенов [3].
Существует и обратная направленность вектора «андрогены-ИР»: ожирение, метаболический синдром, СД2 предрасполагают к развитию андродефицита [4]. С увеличением массы адипоцитов под воздействием ароматазы концентрация циркулирующих эстрогенов возрастает, что приводит к подавлению выработки лютеинизирующего гормона и, следовательно, Т. Висцеральное ожирение также ассоциировано с гиперпродукцией целого ряда гормонов (лептин, цитокины, грелин, инсулин), которые ингибируют ось гипоталамус-гипофиз-яички на разных уровнях и, соответственно, ведут к гипоандрогении [7]. Формирование ИР в условиях недостаточной концентрации андрогенов реализуется через несколько механизмов:
- уменьшение экспрессии инсулиновых рецепторов;
- уменьшение экспрессии субстратов инсулиновых рецепторов, а также их фосфорилирования;
- уменьшение активности ключевых ферментов, открывающих пути утилизации глюкозы через пентозофосфатный путь и цикл трикарбоновых кислот;
- недостаточная активность процессов окислительного фосфорилирования, липидного окисления с внутриклеточной аккумуляцией триглицеридов в скелетных мышцах [8].
При сравнении мужчин с наличием андродефицита и без него в проекте TELECOM обнаружено, что первые имели более высокие показатели триглицеридов, холестерина липопротеидов низкой плотности, общего холестерина, индекса массы тела, соотношения окружность талии/окружность бедер, систолического артериального давления, уровня глюкозы и инсулина натощак и через 2 ч после еды и более низкие уровни α-холестерина. При применении метода мультивариантного анализа после поправки с учетом индекса массы тела и соотношения талия/бедро только уровни инсулина и триглицеридов оставались статистически значимо различными между группами, что свидетельствует о возможности самостоятельного влияния Т на обмен инсулина, независимо от других метаболических изменений [9]. Эти данные в последующем были подтверждены и в различных возрастных группах: для мужчин среднего и пожилого возраста [10].
В этой связи с практических позиций высоковероятно позитивное влияние заместительной терапии Т на чувствительность к инсулину. Действительно, в одной из недавних работ сравнивали выраженность ИР, которую оценивали по скорости внутривенной инфузии глюкозы во время проведения эугликемического гиперинсулинемического клэмпа, в группах мужчин с гипогонадотропным гипогонадизмом и без него. У мужчин с гипогонадизмом скорость инфузии была меньше на 36%; здесь же было отмечено снижение экспрессии инсулиновых рецепторов, субстрата инсулиновых рецепторов и белков-транспортеров GLUT4. При лечении этих пациентов внутримышечными препаратами Т обнаружили увеличение экспрессии указанных выше рецепторов и белков-переносчиков наряду с улучшением чувствительности к инсулину (повышение скорости инфузии глюкозы на 32%) [11].
В противовес разделяемой большинством исследователей точке зрения о благоприятном влиянии андрогенов у мужчин на сенситивность к инсулину и углеводный обмен, E.J. Gianatti и соавт. (2014) опубликовали несколько иные результаты: по их данным, терапия Т не оказывала благоприятного влияния ни на ИР, оценивавшуюся по индексу HOMA1, ни на гликемический контроль [12]. Проведенный мета-анализ семи рандомизированных контролируемых исследований, в пяти из которых использовался индекс HOMA1, подтвердил теорию снижения ИР на фоне лечения Т; впрочем, две работы с использованием HOMA2 (модифицированного индекса ИР) говорят об отсутствии какого-либо эффекта [13]. Таким образом, влияние андрогенов на ИР все еще не совсем понятно. Несмотря на то, что дизайн исследований схож, результаты их довольно противоречивы. Одним из объяснений сложившейся дихотомии могут являться разнонаправленные эффекты эндо- и экзогенных гормонов, а также различных видов и доз препаратов андрогенов.
У женщин, в отличие от мужчин, вопрос о влиянии андрогенов на процессы ИР практически не изучен. Большинство таких работ проведено на пациентках с синдромом поликистозных яичников (СПКЯ). Это заболевание является типичным примером гиперандрогенного состояния и встречается в популяции в 7–11% случаев среди женщин фертильного возраста. В течение 20 лет наблюдения около 20% таких пациенток заболевают СД2 [14]. Однако у женщин с СПКЯ, помимо гиперандрогении, имеется ряд других факторов, способствующих развитию и прогрессированию ИР, – ожирение, дислипидемия, артериальная гипертония, нарушение фибринолиза. Наряду с этим, фенотипическая изменчивость этого синдрома определяет весьма гетерогенный профиль сочетания продиабетогенных состояний у каждого конкретного индивидуума [14, 15].
Определить точку отсчета формирования порочного круга «ИР-гиперандрогения» достаточно проблематично. Согласно современным воззрениям, первоосновой синдрома стромального гипертекоза яичников является ИР [16], и высокий уровень андрогенов является лишь одним из ее проявлений [17]. Инсулин и лютеинизирующий гормон выступают как синергисты, стимулируя синтез андрогенов в тека-клетках через активацию цитохрома P450C17α. Описаны и экстраовариальные механизмы развития гиперандрогении при гипер инсулинемии:
- стимуляция активности P450C17α в надпочечниках;
- подавление продукции печенью белка, связывающего половые гормоны, что приводит к увеличению концентрации свободного Т;
- стимуляция выброса ЛГ в гипофизе [18].
Ряд исследовательских работ различной давности, напротив, склоняется к первичности гиперандрогении. В недавнем исследовании самок мышей после овариоэктомии лечили 5-дигидроэпиандростероном и наблюдали снижение экспрессии GLUT4, повышение уровней глюкозы крови и степени ИР [19]. Другим свидетельством в пользу первостепенности гиперандрогении является снижение ИР под действием антиандрогенной терапии спиронолактоном, флутамидом, бусерелином [20]. Важно подчеркнуть, что в последней работе использовалась оценка ИР с помощью клэмпа – золотого стандарта ее диагностики.
Современные исследования, изучающие связь между уровнями Т и ИР у женщин без СПКЯ, малочисленны. В частности, обнаружено, что у беременных наблюдается положительная корреляция между повышенным уровнем Т и ИР [21]. Гиперандрогения ассоциирована с риском развития метаболического синдрома и, следовательно, ИР у пре- и постменопаузальных женщин [22]. В нашей работе у женщин с ишемической болезнью сердца (ИБС) гиперандрогения была ассоциирована с ранним развитием ИР (оценка проводилась по уровню базальной инсулинемии и индекса HOMA1) уже в возрасте 35–55 лет. В возрастной категории 55–65 лет у пациенток с концентрацией Т ≥3 нмоль/л, в отличие от сверстниц с нормоандрогенией, зафиксировано также увеличение глюкозы плазмы, медиана которой (7,2 (5,5; 8,8) ммоль/л) превышала диагностические для СД2 значения, иллюстрируя содружественное негативное влияние возраста и высокого уровня андрогена на уровень гликемии. Полученные результаты были достоверны в парциальном корреляционном анализе с контролем роста и массы тела [1].
Подводя некий промежуточный итог анализа данных, необходимо констатировать сохраняющуюся необходимость дальнейшего изучения взаимоотношений андрогенов с инсулинорезистентным кластером у женщин, не страдающих СПКЯ. Однако пациентки с гиперандрогенией 56–65 лет, имеющие ИБС, уже сегодня нуждаются в регулярном мониторинге гликемии и наблюдении с «диабетической настороженностью».
Женские половые гормоны и инсулинорезистентность
Установлен целый ряд механизмов, связывающих эстрадиол с повышенной чувствительностью к инсулину у женщин. В частности, 17-бета-этинил-эстрадиол предотвращает аккумуляцию жира посредством супрессии липогенеза, в том числе в печени, и активации липолиза; в скелетной мускулатуре эстрадиол усиливает утилизацию глюкозы, модулируя экспрессию транспортеров глюкозы GLUT4 [23]. Описаны прямые протекторные эффекты эстрогенов в отношении поджелудочной железы, их способность снижать чувствительность к глюкагону и выраженность его секреции, что, в свою очередь, уменьшает глюкагон-индуцированную гипергликемию [23, 24].
Представляется интересной одна из последних работ, выполненная на животных моделях, где показано, что у самок новозеландских мышей с ожирением эстрогены защищают β-клеточный аппарат поджелудочной железы от разрушения, снижая его чувствительность к глюколипотоксическим состояниям [24]. Авторы предполагают большую выраженность этого эффекта у самок, нежели у самцов, так как у первых связанные с G-белком эстрогеновые рецепторы, предотвращающие апоптоз панкреатических клеток, в значительно большем количестве экспрессируются в островковых клетках поджелудочной железы.
Классическая концепция менопаузы строится на том, что в этом периоде на фоне эстрогеновой недостаточности организм женщины особенно уязвим в отношении прогрессирования атерогенеза, артериальной гипертензии, нарушений липидного, углеводного обмена, ожирения и коагуляционного гомеостаза [25, 26, 27]. C другой стороны, по мнению F. Lizcano, G. Guzmán (2014), первостепенность эстрогенов в развитии метаболических заболеваний во время менопаузы представляется спорной, возможно, ключом к проблеме служит нарушенный обмен андрогенов [28]; аналогичной позиции придерживаются J.S. Brand, Y.T. van der Schouw (2010) [29].
C. Kim и соавт. (2015) при изучении восьми проспективных обсервационных исследований у женщин резюмировали, что у женщин высокий эстрадиол чаще, чем низкий, был ассоциирован с сердечно-сосудистым риском. Авторы считают, что механизм действия половых гормонов, в частности эстрадиола, может быть опосредован геномными, негеномными эффектами, воздействием на общепринятые и другие, менее изученные факторы риска [30]. Предполагается, что действие эстрогенов на сосуды, по крайней мере отчасти, зависит от выраженности атеросклероза. Так, установлено, что экспрессия рецепторов к эстрадиолу значительно снижена в очагах атеротромбоза, в связи с чем прямые эффекты эстрогенов, зависимые от их влияния на рецепторы, в таких артериях будут проявляться в меньшей степени или даже отсутствовать. Возможность разнонаправленного эффекта эстрадиола в зависимости от степени атеросклеротического поражения сосуда разделяют также и отечественные авторы [31]. Учитывая тесную патогенетическую связь эндотелиальной дисфункции и ИР, можно предполагать вклад описанных механизмов и в развитие углеводных нарушений, однако подтверждение или опровержение подобных идей требует дальнейших научных изысканий.
Возвращаясь к вопросам ИР как таковой, необходимо отметить возможность ее раннего развития у плода любого пола на фоне эстрогендефицита у матери, продемонстрированную на приматах [32]. Возможно, эстрогены оказывают благоприятное воздействие на ИР как у мужчин, так и у женщин. В исследовании на крысах терапия эстрогенами снижала показатели HOMA1 у животных обоих полов [33]. Аналогично, в работе А. Inada и соавт. (2016) у самцов мышей, подвергнутых орхиэктомии, терапия эстрогенами усиливала экспрессию GLUT4 и их транслокацию к клеточной мембране, что снижало уровень гликемии и степень ИР [19].
Интересна эволюция чувствительности к инсулину, наблюдаемая у лиц обоих полов во время пубертата. С наступлением подросткового возраста у юношей чувствительность к инсулину снижается, несмотря на уменьшение процентного количества жировой ткани и увеличения мышечной. У девушек количество жировой ткани, напротив, достоверно увеличивается, однако сенситивность к инсулину значимо не изменяется. Транзиторное снижение чувствительности к инсулину у юношей может быть объяснено развитием относительного дефицита эстрогенов на фоне уменьшения соотношения эстрадиол/Т [34].
Таким образом, в мужском организме не только андрогены, но и эстрогены модулируют клиническое течение и патофизиологические механизмы развития ИР. Концентрация эстрадиола в крови здоровых молодых мужчин, положительно коррелируя с уровнем Т, сравнима с эстрогенной насыщенностью у женщин в ранней фолликулярной фазе менструального цикла и значительно превышает аналогичные уровни у женщин в постменопаузе [1]. Исследование Antonio с участием 3369 европейских мужчин не выявило какой-либо корреляции между базальным уровнем эстрадиола и развитием метаболических нарушений, хотя в многофакторном анализе более низким значениям соотношения эстрадиол/T соответствовала меньшая вероятность наличия метаболического синдрома. Таким образом, возможно, у взрослых мужчин определяющее значение имеют не абсолютные уровни эстрадиола, а его соотношение с Т [35]. По мнению J. Tőke и соавт. (2014), именно патологическое повышение концентрации Е2 у мужчин приводит к метаболическим нарушениям, включая резистентность к инсулину и СД2, как непосредственно, так и косвенно, за счет снижения концентрации общего и биодоступного Т [36]; аналогичную позицию разделяет G. Williams (2012) [37].
Интересно, что и низкое содержание эстрогенов у мужчин тоже может быть ассоциировано с ИР. Врожденный дефект ароматазы – уникальная модель для изучения роли эстрогенов у мужчин – состояние, характеризующееся изолированным дефицитом эстрогенов на фоне нормального содержания андрогенов, сопряжено с наличием ИР, остеопороза, выраженной дислипидемии и формированием стеатогепатоза [38].
Лептин, адипонектин и половые гормоны
Жировая ткань – активный продуцент адипоцитокинов. Некоторые адипокины, например лептин, попадают в системный кровоток (и оказывают системные эффекты), в то время как другие, такие как фактор некроза опухоли-α, интерлейкин-6 и ингибитор активатора плазминогена, локализуются в жировой ткани и функционируют как паракринные или аутокринные регуляторы [39]. Лептин занимает особое место в ряду адипоцитокинов, оказывая регуляторное влияние на различные физиологические процессы, включающие аппетит, массу тела, нейроэндокринные функции, уровень гликемии. Он воздействует на симпатическую и парасимпатическую нервные системы, что приводит к усиленному поглощению глюкозы мышечными клетками, снижению панкреатического синтеза глюкагона и печеночной продукции глюкозы [40]. Благодаря лептину происходит диалог между жировой тканью и гипоталамусом, его называют «голосом жировой ткани» [16]. В последнее время получены данные о возможности секреции лептина плацентой и яичниками, что свидетельствует о его роли в регуляции репродуктивной системы и развитии СПКЯ [41].
Действительно, лептин находится в динамическом балансе с уровнем половых гормонов: он может напрямую влиять на концентрацию эстрадиола, который, в свою очередь, регулирует продукцию лептина адипоцитами по механизму положительной обратной связи [16]. У женщин лептин выступает в качестве индикатора нутриционного статуса, необходимого для зачатия и успешного протекания беременности, активации оси гипоталамус-гипофиз-яичники, что было впервые изучено на моделях мышей с нокаутом соответствующего гена. Экзогенное введение лептина таким животным индуцировало половое созревание, развитие гонад, нормализовало секрецию гонадотропинов и восстанавливало фертильность. В экспериментальных работах введение лептина женщинам с его дефицитом также приводило к увеличению концентраций гонадотропинов и эстрадиола [42, 43].
Было высказано предположение, что лептин меньше эволюционировал как гормон сытости и больше – как сигнал для репродуктивной системы об адекватном запасе энергии. Уровень лептина повышается на 50% непосредственно перед началом полового созревания, в дальнейшем наблюдается его стабилизация на протяжении 2 лет. Для девочек характерен стойкий подъем уровня лептина на протяжении всего пубертатного периода с более высокими показателями на поздних стадиях, что соотносится с увеличением эстрогенов [44]. Изменяя секрецию лютеинизирующего гормона, лептин участвует в формировании нарушений менструального цикла при голодании [45]. При адекватном нутритивном статусе лептин усиливает эффекты гонадотропинов, инсулина и соматомедина на стероидогенез в тканях яичника и созревание женских половых клеток – ооцитов [46]. Ожирение сопровождается сложной нейро-гормональной реакцией, нарушающей пути сигнальной трансдукции лептина с развитием лептинорезистентности, ведущей, в свою очередь, к деактивации системы гипоталамус-гипофиз-яичники, нарушению менструального цикла, созревания ооцитов и фолликулов, процессов стероидогенеза в гранулезных и тека-клетках яичников [47].
Примечательно, что у женщин с ожирением уровень лептина выше, чем у мужчин с аналогичным ИМТ [16], что обусловлено специфичным для пола профилем половых стероидов. Актуальность исследования взаимоотношений лептина и андрогенов не вызывает сомнений ввиду неуклонного роста частоты ожирения, ИР и бесплодия в мужской популяции. Вербицкая О.Г. и соавт. (2013) изучали уровень лептина и андрогенов у мальчиков и подростков с ожирением. По их мнению, выявленная на стадии препубертата гиперлептинемия является важным физиологическим регулятором сигнала к началу полового созревания. Повышенный уровень лептина у мальчиков с ожирением в пубертатном возрасте, а также сохраняющаяся повышенная концентрация антимюллерова гормона, подавляя подъем уровня андрогенов, обусловливает у них развитие пролонгированного пубертата [48].
Гиперлептинемия может привести к глубоким нарушениям репродуктивной системы мужчин с ожирением. Она индуцирует клинический андрогенный дефицит за счет снижения чувствительности андрогеновых рецепторов к Т и блокады синтеза лютеинизирующего гормона в гипофизе, с одной стороны, наряду с усилением ароматизации Т на периферии в эстрадиол под влиянием ароматазы жировой ткани – с другой. Синергичный эффект на выработку андрогенов оказывает активизация в условиях лептинорезистентности окислительного стресса на фоне избытка свободных жирных кислот и триглицеридов в крови [49].
Локальное нарушение выработки лептина у мужчин с отложением жира в мошонке может быть, по мнению некоторых исследователей, важной причиной нарушения сперматогенеза и андродефицита. Они предположили, что скротальный липоматоз ведет к повышению температуры мошонки посредством избыточной жировой изоляции, венозного застоя и высокого расположения яичка в мошонке на фоне ожирения [50].
В 1995–1996 гг. независимыми группами японских и американских ученых был открыт еще один белковый гормон, синтезируемый белыми адипоцитами, – адипонектин, название которого имеет многочисленные синонимы: ACRp30 (adipocyte complement-related protein 30 kDa), adipoQ и GBP28 (gelatin binding protein 28 kDa). Адипонектин обладает противовоспалительным и антиатерогенным действием, что объясняет его отрицательную корреляцию с массой жировой ткани [44]. Вместе с тем уровень адипонектина как у здоровых, так и больных СД2 женщин выше, чем у мужчин [51]. С возрастом плазменная концентрация адипонектина у женщин значительно не меняется. С другой стороны, мужчины старше 70 лет имеют значительно более высокие уровни адипонектина, чем те, кто не достиг этого возраста. Эти данные позволяют предположить, что уровни эстрогенов не оказывают влияния на концентрацию адипонектина, а андрогены подавляют его секрецию [52].
Солнцева А.В. и соавт. (2011) детально изучили гендерные различия адипонектина у детей с алиментарным ожирением и обнаружили более высокие уровни у мальчиков в пубертатном возрасте в сравнении с девочками. Пиковые концентрации были отмечены у мальчиков в периоде раннего пубертата со снижением их к завершению полового созревания, что авторы объясняют отрицательным влиянием повышенного уровня тестикулярных андрогенов на продукцию адипоцитокина. У девочек с развитием пубертата выявлено уменьшение показателей адипонектинемии [53].
Известно, что у женщин адипонектин регулирует выработку гормонов и экспрессию генов в соматотрофах и гонадотрофах гипофиза, ингибируя секрецию лютеинизирующего гормона, но не оказывает влияния на концентрации фолликулотропина. Также адипонектин способен подавлять образование Т в яичниках [44]. В недавнем исследовании у взрослых женщин с СПКЯ при изучении в рамках кластерного анализа корреляций 30 адипоцитокинов, ростовых факторов, растворимых молекул адгезии, лизосомальных протеаз с андрогенами, лептин и адипонектин продемонстрировали самые сильные независимые связи [54].
Значимая роль дефицита адипонектина для формирования ИР именно в женской, но не в мужской популяции обнаружена G.A. Bonneau и соавт. (2014) [55]. L.D. Høeg и соавт. (2013), напротив, пишут о том, что уровень плазменного адипонектина ассоциирован с фосфорилированием АМФ-активируемой протеинкиназы только у мужчин. Также у женщин имеется более низкая экспрессия AdipoR1 в скелетных мышцах и более низкая концентрация адипонектинчувствительных мышечных волокон 2 типа, детерминирующие меньшую чувствительность женщин к действию адипонектина [56]. Таким образом, можно заключить, что гормоны жировой ткани как компоненты инсулин-глюкозного гомеостаза, разнонаправленно изменяясь, участвуют в выработке и функционировании половых гормонов на различных этапах становления и функционирования репродуктивной системы, вплоть до ее угасания, как прямо, так и опосредованно. Детализация этих взаимоотношений является предметом дальнейшего изучения.
Глюкозурия и половые гормоны
В физиологических условиях почки фильтруют до 180 г глюкозы в сутки, при этом практически вся она полностью реабсорбируется с помощью натрий-зависимых котранспортеров глюкозы (sodium-glucose cotransporter – SGLT) в проксимальных извитых канальцах. Выделяют 11 типов таких переносчиков, среди которых первостепенное значение имеют SGLT 2 типа (SGLT2), расположенные в S1-сегменте проксимального извитого канальца и осуществляющие реабсорбцию до 90% профильтрованной глюкозы. Остальные 10% глюкозы реабсорбируются SGLT 1 типа (SGLT1) в S2- и S3-сегментах проксимальных извитых канальцев. Молекулы глюкозы, поступившие в эпителиальные клетки почечных канальцев, связываются глюкозными транспортерами (GLUT) и с помощью пассивного транспорта выделяются в кровь [57].
В связи с появлением принципиально нового класса органопротективных и прогнозмодифицирующих сахароснижающих препаратов, механизм действия которых автономен от инсулина и сенситивности тканей к нему, представляет интерес возможность его индивидуального эффекта в зависимости от пола. В исследованиях на мышах было обнаружено, что самки имеют большую концентрацию белков-транспортеров GLUT и экспрессию рецепторов SGLT, чем самцы [58, 59]. Проведенная овариоэктомия не оказывала никакого влияния на количество натрий-зависимых котранспортеров глюкозы [60]. Кастрация самцов ассоциировалась с увеличением экспрессии SGLT1, а дальнейшая заместительная терапия Т приводила к обратному эффекту. Выявленные половые различия, по мнению авторов, ассоциированы с ингибирующим влиянием андрогенов. Более поздняя работа, где исследовался 2 тип SGLT, в целом подтверждает эти данные: экспрессия транспортера выше у самок мышей и снижается при лечении андрогенами самцов мышей после кастрации. Однако лечение эстрадиолом самок после овариоэктомии все же увеличивало экспрессию SGLT2 [60]. В этой связи теоретически можно предполагать меньшую предрасположенность женщин к глюкозурии наряду с большей эффективностью у них ингибиторов SGLT. Несмотря на это, результаты крупных проектов последних лет: EMPA-REG OUTCOME, CVD-REAL, CANVAS свидетельствуют об отсутствии различий в сахароснижающем эффекте на фоне терапии натрий-глюкозными котранспортерами у лиц с СД2 различного пола.
Заключение
Взаимосвязь между ожирением и нарушением фертильности у мужчин и женщин давно доказана, однако изучение уровня андрогенов и эстрогенов сегодня выходит за рамки репродуктивной медицины. В связи с надвигающейся пандемией СД и ожирения представляет интерес изучение дополнительных, «неклассических» факторов риска и аспектов патогенеза этих нозологий, в частности, дисбаланса основных половых гормонов у лиц обоих полов с более глубоким пониманием патогенетических механизмов, обуславливающих гендерспецифические различия в развитии и исходах нарушений углеводного обмена. Уточнение индивидуального профиля риска пациентов с ИР/гипергликемией, включающего андрогены и эстрогены, позволит выявить уязвимые звенья для активного медикаментозного и немедикаментозного воздействия. Планирование и проведение в будущем рандомизированных контролируемых исследований с «твердыми конечными точками» может открыть новые горизонты в использовании половых гормонов или их модуляторов в терапии и профилактике хронических неинфекционных заболеваний.
Дополнительная информация
Источник финансирования. Поисково-аналитическая работу осуществлена на личные средства авторского коллектива.
Конфликт интересов. Авторы декларируют отсутствие явных и потенциальных конфликтов интересов, связанных с публикацией настоящей статьи.
1. Цыганкова О.В. Этиопатогенетические особенности ишемической болезни сердца в зависимости от уровня половых гормонов, пола и возраста: Дис. … док. мед. наук. – Новосибирск; 2016. [Tsygankova OV. Etiopatogeneticheskie osobennosti ishemicheskoi bolezni serdtsa v zavisimosti ot urovnya polovykh gormonov, pola i vozrasta. [dissertation] Novosibirsk; 2016. (In Russ).] Доступно по: http://rsmu.ru/fileadmin/rsmu/img/about_rsmu/disser/8/d_cygankova_ov.pdf. Ссылка активна на 09.04.2017.
2. Liu D, Iruthayanathan M, Homan LL, et al. Dehydroepiandrosterone Stimulates Endothelial Proliferation and Angiogenesis through Extracellular Signal-Regulated Kinase 1/2-Mediated Mechanisms. Endocrinology. 2008;149(3):889-898. doi: 10.1210/en.2007-1125.
3. Bekaert M, Van Nieuwenhove Y, Calders P, et al. Determinants of testosterone levels in human male obesity. Endocrine. 2015;50(1):202-211. doi: 10.1007/s12020-015-0563-4.
4. Haring R, Ittermann T, Völzke H, et al. Prevalence, incidence and risk factors of testosterone deficiency in a population-based cohort of men: results from the study of health in Pomerania. The Aging Male. 2010;13(4):247-257. doi: 10.3109/13685538.2010.487553.
5. Stellato RK, Feldman HA, Hamdy O, et al. Testosterone, sex hormone-binding globulin, and the development of type 2 diabetes in middle-aged men: prospective results from the Massachusetts male aging study. Diabetes Care. 2000;23(4):490-494. doi: 10.2337/diacare.23.4.490.
6. Høst C, Gormsen LC, Hougaard DM, et al. Acute and Short-term Chronic Testosterone Fluctuation Effects on Glucose Homeostasis, Insulin Sensitivity, and Adiponectin: A Randomized, Double-Blind, Placebo-Controlled, Crossover Study. J. Clin. Endocr. Metab. 2014;99(6):E1088-E1096. doi: 10.1210/jc.2013-2807.
7. Grossmann M. Testosterone and glucose metabolism in men: current concepts and controversies. J. Endocrinol. 2013;220(3):R37-R55. doi: 10.1530/joe-13-0393.
8. Rao PM, Kelly DM, Jones TH. Testosterone and insulin resistance in the metabolic syndrome and T2DM in men. Nature Reviews Endocrinology. 2013;9(8):479-493. doi: 10.1038/nrendo.2013.122.
9. Simon D, Charles M-A, Nahoul K, et al. Association between Plasma Total Testosterone and Cardiovascular Risk Factors in Healthy Adult Men: The Telecom Study1. J. Clin. Endocr. Metab. 1997;82(2):682-685. doi: 10.1210/jcem.82.2.3766.
10. Zhang N, Zhang H, Zhang X, et al. The relationship between endogenous testosterone and lipid profile in middle-aged and elderly Chinese men. European journal of endocrinology / European Federation of Endocrine Societies. 2014;170(4):487-494. doi: 10.1530/eje-13-0802.
11. Dhindsa S, Ghanim H, Batra M, et al. Insulin Resistance and Inflammation in Hypogonadotropic Hypogonadism and Their Reduction After Testosterone Replacement in Men With Type 2 Diabetes. Diabetes Care. 2016;39(1):82-91. doi: 10.2337/dc15-1518.
12. Gianatti EJ, Dupuis P, Hoermann R, et al. Effect of Testosterone Treatment on Glucose Metabolism in Men With Type 2 Diabetes: A Randomized Controlled Trial. Diabetes Care. 2014;37(8):2098-2107. doi: 10.2337/dc13-2845.
13. Grossmann M, Hoermann R, Wittert G, Yeap BB. Effects of testosterone treatment on glucose metabolism and symptoms in men with type 2 diabetes and the metabolic syndrome: a systematic review and meta-analysis of randomized controlled clinical trials. Clin. Endocrinol. (Oxf.). 2015;83(3):344-351. doi: 10.1111/cen.12664.
14. Macut D, Antić IB, Bjekić-Macut J. Cardiovascular risk factors and events in women with androgen excess. J. Endocrinol. Invest. 2014;38(3):295-301. doi: 10.1007/s40618-014-0215-1.
15. Stuckey BGA, Opie N, Cussons AJ, et al. Clustering of metabolic and cardiovascular risk factors in the polycystic ovary syndrome: a principal component analysis. Metabolism. 2014;63(8):1071-1077. doi: 10.1016/j.metabol.2014.05.004.
16. Сметник В.П. Половые гормоны и жировая ткань // Ожирение и метаболизм. — 2007. — Т. 4. — №3. — C. 17-22. [Smetnik VP. Polovye gormony i zhirovaya tkan’. Obesity and metabolism. 2007;4(3):17-22. (In Russ).] doi: 10.14341/2071-8713-5017
17. Гамидов С.И., Иремашвили В.В. Метаболический синдром в урологии. М.: Издательство Инсайт Полиграфик; 2010. [Gamidov SI, Iremashvili VV. Metabolicheskii sindrom v urologii. Moscow: Insait Poligrafik; 2010. (In Russ).]
18. Barber TM, Dimitriadis GK, Andreou A, Franks S. Polycystic ovary syndrome: insight into pathogenesis and a common association with insulin resistance. Clin. Med. (Northfield Il.). 2016;16(3):262-266. doi: 10.7861/clinmedicine.16-3-262.
19. Inada A, Fujii NL, Inada O, et al. Effects of 17β-Estradiol and Androgen on Glucose Metabolism in Skeletal Muscle. Endocrinology. 2016;157(12):4691-4705. doi: 10.1210/en.2016-1261.
20. Moghetti P, Tosi F, Castello R, et al. The insulin resistance in women with hyperandrogenism is partially reversed by antiandrogen treatment: evidence that androgens impair insulin action in women. J. Clin. Endocr. Metab. 1996;81(3):952-960. doi: 10.1210/jcem.81.3.8772557.
21. Villarroel C, Salinas A, López P, et al. Pregestational type 2 diabetes and gestational diabetes exhibit different sexual steroid profiles during pregnancy. Gynecol. Endocrinol. 2016;33(3):212-217. doi: 10.1080/09513590.2016.1248933.
22. Valderhaug TG, Hertel JK, Nordstrand N, et al. The association between hyperandrogenemia and the metabolic syndrome in morbidly obese women. Diabetol. Metab. Syndr. 2015;7(1). doi: 10.1186/s13098-015-0040-5.
23. Jelenik T, Roden M. How Estrogens Prevent From Lipid-Induced Insulin Resistance. Endocrinology. 2013;154(3):989-992. doi: 10.1210/en.2013-1112.
24. Vogel H, Mirhashemi F, Liehl B, et al. Estrogen Deficiency Aggravates Insulin Resistance and Induces β-Cell Loss and Diabetes in Female New Zealand Obese Mice. Horm. Metab. Res. 2013;45(06):430-435. doi: 10.1055/s-0032-1331700.
25. Dehlendorff C, Andersen KK, Olsen TS. Sex Disparities in Stroke: Women Have More Severe Strokes but Better Survival Than Men. Journal of the American Heart Association. 2015;4(7):e001967. doi: 10.1161/jaha.115.001967.
26. Sciacqua A, Perticone M, Tassone EJ, et al. Uric acid is an independent predictor of cardiovascular events in post-menopausal women. Int. J. Cardiol. 2015;197:271-275. doi: 10.1016/j.ijcard.2015.06.069.
27. Smith GN. The Maternal Health Clinic: Improving women’s cardiovascular health. Semin. Perinatol. 2015;39(4):316-319. doi: 10.1053/j.semperi.2015.05.012.
28. Lizcano F, Guzmán G. Estrogen Deficiency and the Origin of Obesity during Menopause. BioMed Research International. 2014;2014:1-11. doi: 10.1155/2014/757461.
29. Brand JS, van der Schouw YT. Testosterone, SHBG and cardiovascular health in postmenopausal women. Int. J. Impot. Res. 2010;22(2):91-104. doi: 10.1038/ijir.2009.64.
30. Kim C, Cushman M, Kleindorfer D, et al. A Review of the Relationships between Endogenous Sex Steroids and Incident Ischemic Stroke and Coronary Heart Disease Events. Curr. Cardiol. Rev. 2015;11(999):1-1. doi: 10.2174/1573403×11666150107160016.
31. Лебедева А.Ю., Клыков Л.Л., Зайцева В.В. ИБС у молодых женщин: проблемы диагностики и профилактики // Российский кардиологический журнал. – 2011. – №6 – С. 90-97. [Lebedeva AY, Klykov LL, Zaitseva VV. Coronary heart disease in young women: problems of diagnostics and prevention. Russian Journal of Cardiology. 2011;(6):90-97. (In Russ.)] doi: 10.15829/1560-4071-2011-6-90-97
32. Maniu A, Aberdeen GW, Lynch TJ, et al. Estrogen deprivation in primate pregnancy leads to insulin resistance in offspring. J. Endocrinol. 2016;230(2):171-183. doi: 10.1530/joe-15-0530.
33. Pratchayasakul W, Chattipakorn N, Chattipakorn SC. Effects of estrogen in preventing neuronal insulin resistance in hippocampus of obese rats are different between genders. Life Sci. 2011;89(19-20):702-707. doi: 10.1016/j.lfs.2011.08.011.
34. Moran A, Jacobs DR, Steinberger J, et al. Changes in Insulin Resistance and Cardiovascular Risk During Adolescence: Establishment of Differential Risk in Males and Females. Circulation. 2008;117(18):2361-2368. doi: 10.1161/circulationaha.107.704569.
35. Antonio L, Wu FCW, O’Neill TW, et al. Associations Between Sex Steroids and the Development of Metabolic Syndrome: A Longitudinal Study in European Men. J. Clin. Endocr. Metab. 2015;100(4):1396-1404. doi: 10.1210/jc.2014-4184.
36. Tőke J, Czirják G, Bezzegh A, et al. Effects and significance of estradiol in men. Orv. Hetil. 2014;155(23):891-896. doi: 10.1556/oh.2014.29914.
37. Williams G. Aromatase up-regulation, insulin and raised intracellular oestrogens in men, induce adiposity, metabolic syndrome and prostate disease, via aberrant ER-α and GPER signalling. Mol. Cell. Endocrinol. 2012;351(2):269-278. doi: 10.1016/j.mce.2011.12.017.
38. McDermott MT. Endocrine secrets. 6th ed. Philadelphia: Saunders; 2013.
39. Michalakis K, Mintziori G, Kaprara A, et al. The complex interaction between obesity, metabolic syndrome and reproductive axis: A narrative review. Metabolism. 2013;62(4):457-478. doi: 10.1016/j.metabol.2012.08.012.
40. Coppari R, Bjørbæk C. Leptin revisited: its mechanism of action and potential for treating diabetes. Nature Reviews Drug Discovery. 2012;11(9):692-708. doi: 10.1038/nrd3757.
41. Hausman GJ, Barb CR. Adipose Tissue and the Reproductive Axis: Biological Aspects. Endocrine development. 2010;19:31-44. doi: 10.1159/000316895.
42. Donato JJ, Cravo RM, Frazão R, Elias CF. Hypothalamic Sites of Leptin Action Linking Metabolism and Reproduction. Neuroendocrinology. 2011;93(1):9-18. doi: 10.1159/000322472.
43. Горбатенко Н.В., Беженарь В.Ф., Фишман М.Б. Влияние ожирения на развитие нарушения репродуктивной функции у женщин (аналитический обзор литературы) // Ожирение и метаболизм. – 2017. – Т.14. – № 1 – С.3-8. [Gorbatenko NV, Bezhenar VF, Fishman MB. Obesity and reproductive health of women. Obesity and metabolism. 2017;14(1):3-8. (In Russ).] doi:10.14341/OMET201713-8
44. Ковалева Ю.В. Гормоны жировой ткани и их роль в формировании гормонального статуса и патогенезе метаболических нарушений у женщин // Артериальная гипертензия. – 2015. – Т.21. – № 4 – С.356-370. [Kovalyova YV. Adipose tissue hormones and their role for female fertility and metabolic disorders. Arterial hypertension. 2015;21(4):356-370. (In Russ).]
45. Santos ED, Pecquery R, Mazancourt Pd, Dieudonné M-N. Adiponectin and Reproduction. Vitam Horm. 2012;90:187-209. doi: 10.1016/b978-0-12-398313-8.00008-7.
46. Michalakis K, Mintziori G, Kaprara A, et al. The complex interaction between obesity, metabolic syndrome and reproductive axis: A narrative review. Metabolism. 2013;62(4):457-478. doi: 10.1016/j.metabol.2012.08.012.
47. Sharma A, Bahadursingh S, Ramsewak S, Teelucksingh S. Medical and surgical interventions to improve outcomes in obese women planning for pregnancy. Best Practice & Research Clinical Obstetrics & Gynaecology. 2015;29(4):565-576. doi: 10.1016/j.bpobgyn.2014.12.003.
48. Вербицкая О.Г., Попова В.А., Афонин А.А., и др. Клинико-диагностическое значение определения лептина и андрогенов у мальчиков и подростков с ожирением // Медицинский вестник Юга России. – 2013. – № 2. – С.37-42. [Verbitskaya OG, Popova VA, Afonin AA, et al. Clinicodiagnostic value of determination of leptin and androgenic hormones in boys and teenagers with obesity. Medical Herald of the South of Russia. 2013;(2):37-43. (In Russ).] doi:10.21886/2219-8075-2013-2-37-43
49. Калинченко С.Ю., Тюзиков И.А., Ворслов Л.О., Тишова Ю.А. Ожирение, инсулинорезистентность и репродуктивное здоровье мужчины: патогенетические взаимодействия и современная патогенетическая фармакотерапия // Эффективная фармакотерапия. – 2015. – № 27. – С.66-79. [Kalinchenko SY, Tyuzikov IA, Vorslov LO, Tishova YA. Insulin Resistance and Male Reproductive Health: Pathogenic Interactions and Pathogenetic Pharmacotherapy. Effective Pharmacotherapy. 2015;(27):66-79. (In Russ).]
50. ShaflK A, Olfat S. Scrotal Lipomatosis. Br. J. Urol. 1981;53(1):50-54. doi: 10.1111/j.1464-410X.1981.tb03128.x.
51. Aleidi S, Issa A, Bustanji H, et al. Adiponectin serum levels correlate with insulin resistance in type 2 diabetic patients. Saudi Pharmaceutical Journal. 2015;23(3):250-256. doi: 10.1016/j.jsps.2014.11.011.
52. Adamczak M, Rzepka E, Chudek J, Wiecek A. Ageing and plasma adiponectin concentration in apparently healthy males and females. Clin. Endocrinol. (Oxf.). 2005;62(1):114-118. doi: 10.1111/j.1365-2265.2004.02182.x.
53. Солнцева А.В., Аксенова Е.А., Сукало А.В., и др. Гендерные различия и генетический полиморфизм адипонектина у детей с алиментарным ожирением // ВЕСЦІ НАЦЫЯНАЛЬНАЙ АКАДЭМІІ НАВУК БЕЛАРУСІ. СЕРЫЯ МЕДЫЦЫНСКІХ НАВУК. – 2011. – № 2. – С.29-37. [Solntseva AV, Askionova EA, Sukalo AV, et al. Gender changes and genetic polymorphism of adiponectin in children with obesity. Vestsі natsyyanal’nai Akademіі Navuk belarusі. Seryya medytsynskіkh navuk. 2011;(2):29-37. (In Russ).]
54. Baek K-H, Daan NMP, Koster MPH, et al. Biomarker Profiles in Women with PCOS and PCOS Offspring; A Pilot Study. PLoS One. 2016;11(11):e0165033. doi: 10.1371/journal.pone.0165033.
55. Bonneau GA, Pedrozo WR, Berg G. Adiponectin and waist circumference as predictors of insulin-resistance in women. Diabetes & Metabolic Syndrome: Clinical Research & Reviews. 2014;8(1):3-7. doi: 10.1016/j.dsx.2013.10.005.
56. Høeg LD, Sjøberg KA, Lundsgaard A-M, et al. Adiponectin concentration is associated with muscle insulin sensitivity, AMPK phosphorylation, and ceramide content in skeletal muscles of men but not women. J. Appl. Physiol. 2013;114(5):592-601. doi: 10.1152/japplphysiol.01046.2012.
57. Мкртумян А.М., Маркова Т.Н., Мищенко Н.К. Влияние ингибиторов натрий-зависимых котранспортеров глюкозы 2 типа на уровень гликированного гемоглобина и массу тела у больных сахарным диабетом 2 типа // ДОКТОР.РУ. – 2016. – № 3. – С.55-58. [Mkrtumyan AM, Markova TN, Mishchenko NK. Effects of Sodium-Glucose Cotransporter 2 Inhibitors on Glycosylated Hemoglobin Levels and Body Weight in Patients with Type 2 Diabetes Mellitus. Doctor.Ru. 2016;(3):55-58. (In Russ).]
58. Nagao K, Yoshida S, Konishi H. Gender differences in the gene expression profiles of glucose transporter GLUT class I and SGLT in mouse tissues. Die Farmazie. 2014 Nov;69(11):856-9.
59. Sabolić I, Škarica M, Gorboulev V, et al. Rat renal glucose transporter SGLT1 exhibits zonal distribution and androgen-dependent gender differences. American Journal of Physiology-Renal Physiology. 2006;290(4):F913-F926. doi: 10.1152/ajprenal.00270.2005.
60. Sabolić I, Vrhovac I, Eror DB, et al. Expression of Na+-d-glucose cotransporter SGLT2 in rodents is kidney-specific and exhibits sex and species differences. American Journal of Physiology-Cell Physiology. 2012;302(8):C1174-C1188. doi: 10.1152/ajpcell.00450.2011.
Гормон эстрадиол
Эстрадиол – женский половой гормон, самый активный эстроген, который продуцируется преимущественно фолликулярным аппаратом яичников у женщин. В меньших количествах он образуется в яичках и периферических тканях у мужчин и в сетчатой коре надпочечников у обоих полов. Помимо этого, в периоде гестации эстрадиол вырабатывает плацента.
Эстрадиол продуцируется под воздействием лютеинизирующего (ЛГ)и фолликулостимулирующего (ФСГ)гормонов гипофиза, а также пролактина.
Функции эстрадиола
- Развитие плода по женскому типу, формирование вторичных женских половых признаков
- Регуляция менструального цикла
- Активизация кровообращения в матке, повышение свертываемости крови во время беременности
- Участие в процессе сперматогенеза у мужчин
Колебания уровня эстрадиола в менструальном цикле
В начале первой фазы уровень эстрадиола остается достаточно низким, постепенно повышаясь за 3-5 суток до момента овуляции и достигая максимальных значений за час до пикового выброса ЛГ. Продукция гормона осуществляется оболочкой и гранулезными клетками фолликулов.
Спустя 24 часа после овуляции уровень эстрадиола падает , а затем вновь начинает расти до максимума, который фиксируется на 9-е сутки после овуляции. Эстрадиол (совместно с прогестероном) теперь продуцируется желтым телом, образовавшемся на месте фолликула. Если зачатия в менструальном цикле не произошло, желтое тело в яичниках постепенно атрофируется, и уровень эстрогенов падает до минимума, который совпадает с началом менструации.
Как мы видим на графике, в течение менструального цикла уровень гормона дважды повышается, затем понижаясь. Такие колебания называют двухфазной прогрессией эстрадиола.
Референсные значения:
- Фолликулярная фаза: 68-1269 пмоль/л
- Период преовуляции: 131-1655 пмоль/л
- Лютеиновая фаза: 91-861 пмоль/л
Снижение уровня эстрадиола у женщин может свидетельствовать о синдроме Шерешевского-Тернера, гиперпролактинемии, недостаточности лютеиновой фазы, вирильном синдроме (появление у женщины мужских, андрогензависимых черт), хроническом воспалительном процессе в органах малого таза. Кроме того, подобная картина наблюдается при значительных физических нагрузках в случае отсутствия спортивной подготовки, при резком похудении, рационе с преобладанием углеводов и дефицитом жиров, при вегетарианстве, а также во время использования пероральных контрацептивов и приема некоторых медицинских препаратов.
Повышение уровня эстрадиола у женщин возможно при гиперэстрогении, эстрогенсекретирующей опухоли или эндометриоидных кистах в яичниках, циррозе печени, а также в результате приема целого ряда лекарственных препаратов.
У девочек уровень эстрадиола понемногу растет, значительно увеличиваясь в пубертатном периоде.
У женщин в периоде постменопаузы уровень эстрадиола остается неизменно низким, сравнимым с аналогичным показателем у мужчин.
Суточные колебания уровня эстрадиола
Изменения концентрации эстрадиола связано с суточными колебаниями лютеинизирующего гормона (ЛГ). Так, минимальные значения наблюдаются в период между полуночью и 2 часами, а максимум определяется в интервале между 15 и 18 часами.
Эстрадиол во время беременности
Уровень эстрадиола во время беременности повышается, достигая максимума к моменту родов и снижаясь примерно на четвертый день после появления на свет ребенка (в том числе и после кесарева сечения).
Снижение уровня эстрадиола может свидетельствовать об угрозе прерывания беременности вследствие недостаточности функции плаценты.
Референсные значения:
- I триместр: 215-430 пг/мл
- II триметр: 800 – 576 пг/мл
- III триместр: 1810-13900 пг/мл
Хотите записаться на прием?
Повышение и снижение уровня эстрадиола у мужчин
Пониженный уровень эстрадиола у мужчин может наблюдаться при текстикулярной феминизации, гипогонадизме, гиперпролактинемии, хроническом простатите и приеме различных препаратов.
Увеличение концентрации эстрадиола характерно для пациентов с гормонозависимой опухолью яичек и циррозом печени. Помимо этого, подобный результат может быть обусловлен приемом лекарственных препаратов (например, анаболических стероидов).
В норме уровень эстрадиола у мужчин составляет 40-161 пмоль/л.
Анализ на эстрадиол
Анализ на определение эстрадиола (E2) в плазме крови врач может для выявления причин, таких патологий и состояний как:
- Нарушения менструального цикла, в том числе полное отсутствие менструаций (аменорея)
- Отсутствие овуляции в менструальном цикле
- Дисфункциональные маточные кровотечения
- Женское и мужское бесплодие
- ПМС
- Нарушения полового созревания
- Мужской гипогонадизм (состояние, обусловленное недостаточной продукцией андрогенов)
- Женский гирсутизм (избыточный рост волос по мужскому типу)
- Эстрогенсекретирующие (вырабатывающие эстрогены) опухоли у мужчин и женщин
- Остеопороз у женщин
Помимо этого, результат анализа на эстрадиол (в совокупности с другими анализами и методами исследований) дает представление о функционировании фетоплацентарного комплекса (системы мать-плацента-плод) на ранних сроках беременности.
Сдача анализа на эстрадиол требует специальной подготовки!
- Женщины в репродуктивном возрасте проходят исследование на 6-7 день менструального цикла.
- За 2-3 дня необходимо исключить активные физические упражнения и стрессы.
- В день исследования не следует курить.
- Необходимо перенести сдачу анализа при остром воспалительном процессе любой локализации.
- Сдавать анализ на эстрадиол нужно натощак, причем после последнего приема пищи должно пройти как минимум 8, а в идеале – 12 часов. Разрешается употребление воды, но любые другие жидкости (кофе, чай, сок) как с сахаром, так и без него пить запрещено.
Обязательно предупредите вашего врача, если вы принимаете какие-либо лекарственные препараты.
В Нова Клиник вы можете сдать анализы на гормоны в любое удобное для Вас время с понедельника по субботу. Стоимость анализа крови на определение уровня эстрадиола вы можете уточнить в разделе «Цены».
Нужна консультация специалиста?
Низкий эстрадиол у женщин: причины, симптомы, лечение
Гормон эстрадиол оказывает на женский организм значительное влияние. Именно при его непосредственном участии у женщин формируется вся половая система, а также внутренние органы, которые отвечают за репродуктивную функцию организма. Кроме того, эстрадиол оказывает влияние на внешность женщин, наделяя признаками, что отличают их от мужчин: формирует округлые очертания фигуры, грудь, отложения подкожного жира на бедрах и животе.
Не удивительно, что у женщин низкий уровень эстрадиола не только негативно отображается на внешности, но и на темпераменте, менструальном цикле, и что самое главное – на способности забеременеть: показатели эстрадиола ниже нормы нередко свидетельствуют о бесплодии.
Характеристика гормона
Эстрадиол является основным и самым активным женским половым гормоном, который входит в подкласс эстрогенов. Вырабатывается он в большей мере в яичниках, в незначительном количестве – надпочечниками, и основным предназначением его является подготовка женского организма к беременности. Влияет этот гормон также на состояние кожи, отсутствие/наличие морщин, бодрое состояние духа, высокую физическую активность, выносливость. Помимо этого, он:
- стимулирует созревание яйцеклетки;
- влияет на усиление кровотока в матке;
- способствует утолщению внутреннего слизистого слоя матки, ширина которого к моменту выхода яйцеклетки из фолликула должна составлять не менее сантиметра;
- улучшает свертываемость крови;
- ускоряет образование и обновление клеток, тканей, мышц;
- укрепляет сосуды;
- задерживает натрий и воду;
- участвует в обменных процессах в костных тканях;
- понижает уровень холестерина;
- успокаивающе влияет на нервную систему.
Количество эстрадиола в крови нестабильно и постоянно колеблется. Наивысшие показатели фиксируются между тремя-шестью часами дня, наименьшие – с полуночи до двух ночи. На уровень гормона влияет здоровье женщины, а также менструальный цикл: как только один из фолликулов яйцеклетки начинает активно расти, а в нем созревать яйцеклетка, он начинает выделять эстрогены, сигнализируя матке, что пора готовиться к зачатию.
К моменту созревания фолликула уровень эстрадиола в организме оказывается настолько высоким, что гипоталамус, один из отделов головного мозга, дает сигнал гипофизу увеличить выработку гормонов ЛГ и ФСГ, которые отвечают за работу репродуктивной системы организма. В результате всплеска, когда ФСГ и ЛГ достигают в этот момент своих максимальных показателей, фолликул разрывается и созревшая в нем яйцеклетка выходит, начиная двигаться к матке.
После этого уровень эстрадиола спускается к минимуму, а образовавшееся на месте разорванного фолликула желтое тело начинает активно синтезировать прогестерон. Правда, такой спад недолог, и на девятый день уровень эстрадиола снова возрастает, достигая второго пика, правда, намного меньшего, чем при овуляции и снова снижается.
Когда эстрадиол понижен
Развитие многих заболеваний, связанных со сбоями в работе репродуктивной системы, нередко зависит от слишком низкого или высокого уровня эстрадиола. У женщин, которые не ожидают малыша, норма гормона составляет:
- фолликулярная фаза: от 57 до 227 пмоль/л;
- преовуляторный пик: от 127 до 476 пмоль/л;
- лютеиновая фаза: от 77 до 227 пмоль/л.
Данные эти лишь приблизительны, поскольку уровень гормона меняется ежедневно, поэтому при сдаче крови на анализ, нужно сказать специалисту, какой день цикла. Это позволит более точно диагностировать заболевание, если оно имеется.
О низком уровне эстрадиола многие женщины могут даже не догадываться, пока не начинают планировать беременность: по утверждению медиков, при пониженном количестве этого гормона забеременеть, а также выносить ребенка, очень трудно.
Даже если зачатие и произойдет, вероятность выкидыша чрезвычайно высока: эстрадиол оказывает огромное влияние на формирование плаценты, состояние матки, кровообращение в органах малого таза. Также он ответственен за свертываемость крови, снижая при родах кровотечение.
Среди симптомов, сигнализирующих о том, что уровень эстрадиола ниже нормы, и на которые стоит обратить внимание, чтобы своевременно начать лечение, выделяют:
- нерегулярный цикл: частые задержки или слишком раннее наступление месячных;
- боли во время месячных и предменструальный синдром;
- излишняя сухость и чувство жжения во влагалище;
- снижение сексуального влечения;
- упадок сил, бессилие, быстрая утомляемость;
- скачки давления, мигрени;
- резкое снижение массы тела;
- частые растяжения связок и переломы.
В дальнейшем развиваются признаки, на которые женщина не обратить внимания уже не в состоянии. Это изменение фигуры по мужскому типу, когда бедра сужаются, плечи становятся шире, появляются усики, темнеют волосы на подбородке. Настораживает и ситуация, когда женщина долго не может забеременеть при попытках это сделать.
Причины понижения гормона
На понижение эстрадиола у женщин могут повлиять разные причины. Низкий уровень гормона у женщин всегда наблюдается во время менопаузы или после неё. В этом случае это естественный процесс, заложенный природой, когда количество эстрогенов понижается и остаётся на очень низком уровне.
У женщин репродуктивного возраста понижение эстрадиола может быть связано со следующими заболеваниями:
- Гипогонадизм – сбои в функционировании женских половых органов и молочных желез, в результате чего они атрофируются. Причиной недуга могут быть генетическая патология, гипоплазия яичников, излучения, воспалительные процессы, опухоли гипофиза или гипоталамуса и др.;
- Гипофизарный нанизм – недуг характеризуется задержкой линейного роста (карликовость) и физического развития, который был спровоцирован плохой работой гипофиза и слабой выработкой гормонов;
- Гиперпролактинимия – повышенное содержание гормона пролактина в крови, который в период лактации отвечает за выработку молока и задерживает наступление новой беременности. Если высокое количество пролактина не связано с малышом, на повышение гормона влияют опухоли гипофиза или гипоталамуса, гипотиреоз, цирроз, почечная недостаточность, аборты, операции на грудной клетке;
- Недостаточность лютеиновой фазы – уменьшение выработки желтым телом прогестерона;
- Вирильный синдром – появление у женщин вторичных половых признаков из-за избыточного количества андрогенов и атрофия женских половых органов. Часто является следствием опухоли гипофиза, гипоталамуса, надпочечников, яичников;
- Синдром Шерешевского-Тернера – генетическое заболевание, спровоцированное нарушением в структуре Х-хромосомы, которое сопровождается патологиями в развитии внутренних органов и низким ростом;
- Воспалительные процессы внутренних половых органов;
- Возможность выкидыша.
Также низкий уровень эстрадиола может быть вызван курением, спиртными напитками, причем даже их прием в небольших количествах способен вызвать резкое снижение эстрогена. Влияет на его количество и стремление женщин похудеть, когда после многочасовых тренировок, по возвращении домой они подкрепляют силы несбалансированной диетой, например, пустой гречкой и обезжиренным кефиром.
Также общепризнанным фактом является то, что у вегетарианок по сравнению с женщинами, которые едят мясо, уровень пониженного эстрадиола встречается намного чаще.
Ещё одной причиной, способной спровоцировать падение гормона, является прием лекарственных препаратов без согласования с врачом: во многих антибиотиках, кортикостероидов, гормональных препаратах содержатся вещества, оказывающие влияние на эстрогены. Опасны также противозачаточные препараты, если их применять без консультации с гинекологом: впоследствии это может обернуться невозможностью забеременеть.
Решение проблемы
Если анализы показали пониженное количество эстрагенов, чтобы повысить уровень эстрадиола, врач обычно назначает лекарства, которые содержат этот гормон. Такие препараты не только восстанавливают менструальный цикл, но и успешно справляются со многими заболеваниями, спровоцировавших низкий уровень эстрогена. Это поликистоз яичников, бесплодие, применяют при родовой слабости, переношенной беременности, для снижения уровня пролактина.
В случае обнаружения недуга, с которым содержащие эстрадиол препараты не справляются, назначается лечение, направленное на борьбу с заболеванием. Особенно дело не терпит промедления, если обнаружена раковая опухоль, действия врача в данном случае во многом зависят от недуга и хода течения болезни.
Кроме приема лекарственных препаратов, чтобы повысить уровень эстрадиола в организме, нужно употреблять белковую пищу. В рацион может входить нежирное мясо, рыба, птица, яйца, печень, молочные и кисломолочные продукты, если нет противопоказаний. Нежелательно увлекаться углеводами, а также продуктами, в которых содержится много крахмала: кашами, макаронами, хлебом, картофелем, свеклой. Пищу лучше готовить на пару, варить или тушить, от жареных блюд, чтобы повысить эстрадиол, лучше отказаться.
Причины, последствия и варианты лечения
Эстроген — это гормон, который чаще всего ассоциируется с женщинами, хотя мужчины вырабатывают небольшие количества. Снижение уровня эстрогена может вызвать множество проблем со здоровьем и симптомов.
Хотя эстроген в первую очередь связан с женским развитием в период полового созревания и репродуктивного цикла, он влияет на все, от здоровья костей до эмоционального благополучия.
Низкий уровень эстрогенов может развиваться у женщин любого возраста по нескольким причинам.
Краткие сведения о низком уровне эстрогена:
- Эстроген в основном вырабатывается яичниками.
- Низкий уровень эстрогена может оказывать на организм несколько эффектов.
- Женщины с расстройствами пищевого поведения, такими как анорексия, подвергаются более высокому риску низкого уровня эстрогена.
Уровни эстрогена различаются по многим причинам. Любое состояние, которое влияет на яичники или повреждает их, может вызвать снижение уровня эстрогена в организме.
Самым значительным фактором риска низкого уровня эстрогена является возраст.По мере того как женщины стареют и приближаются к менопаузе, снижение уровня эстрогена является нормальным.
Фактически, уровень эстрогена начинает снижаться за несколько лет до наступления менопаузы (фаза, называемая перименопаузой).
Уровни эстрогена также могут снижаться по ряду других причин, в том числе:
- преждевременной недостаточности яичников
- врожденных состояний, таких как синдром Тернера
- заболеваний щитовидной железы
- чрезмерных физических нагрузок
- сильной недостаточной массы тела
- химиотерапии
- низкой функции гипофиза железа
Наличие гормональных проблем в семейном анамнезе также может увеличить риск развития низкого уровня эстрогена у женщины.
Поделиться на Pinterest Возможные симптомы низкого эстрогена включают нерегулярные месячные, бесплодие и депрессию.Эстроген — важный гормон, поэтому его эффекты могут быть весьма разнообразными.
Симптомы низкого эстрогена могут включать следующее:
- Нерегулярные периоды : Эстроген — один из основных гормонов, управляющих менструальным циклом. Низкий уровень эстрогена может привести к задержкам или нерегулярным менструациям.
- Бесплодие : Низкий уровень эстрогена может предотвратить овуляцию и затруднить беременность, что приведет к бесплодию.
- Слабые кости : Эстроген помогает сохранять кости здоровыми и крепкими. По мере снижения уровня эстрогена может произойти потеря костной массы. Например, женщины в постменопаузе имеют повышенный риск развития остеопороза и переломов костей.
- Болезненный половой акт : Эстроген может влиять на вагинальную смазку. Если уровень становится слишком низким, может возникнуть сухость влагалища, что часто приводит к болезненному сексу.
- Приливы : Приливы часто случаются во время менопаузы из-за низкого уровня эстрогена.
- Депрессия : Считается, что эстроген увеличивает уровень серотонина, химического вещества в головном мозге, которое улучшает настроение. Дефицит эстрогена может вызвать снижение уровня серотонина, что способствует перепадам настроения или депрессии.
- Увеличение инфекций мочевыводящих путей : усиление инфекций мочевыводящих путей может происходить из-за истончения ткани уретры, которое может развиваться при снижении уровня эстрогена.
Влияние на вес
Гормоны, включая эстроген, могут влиять на контроль веса и на то, сколько жира откладывается в организме.Низкий уровень эстрогена, например, во время перименопаузы и менопаузы, может способствовать увеличению веса.
Области, где женщины откладывают жир, также могут изменяться во время менопаузы. Обычно у женщин жир откладывается на бедрах и бедрах. Но это меняется по мере падения уровня эстрогена. Согласно журналу Journal of Climacteric , снижение уровня эстрогена в среднем возрасте связано с увеличением абдоминального жира.
Хотя увеличение веса из-за низкого уровня эстрогена является типичным, оно не обязательно должно быть неизбежным.Соблюдение здоровой диеты и регулярные физические упражнения могут помочь женщинам снизить вероятность набора веса.
Диагностика низкого уровня эстрогена часто начинается с медицинского осмотра, истории болезни и анализа симптомов. Контрольные индикаторы низкого уровня эстрогена включают приливы и пропущенные месячные. Но некоторые из этих симптомов могут возникать и в результате других заболеваний, включая проблемы с щитовидной железой.
Чтобы определить причину низкого уровня эстрогена, врач может сделать анализ крови для проверки уровня гормонов.Врач также может порекомендовать дополнительные тесты, чтобы исключить другие состояния, которые могут вызывать симптомы, похожие на низкий уровень эстрогена.
Не всем женщинам требуется лечение от низкого уровня эстрогена. Но если симптомы низкого уровня эстрогена беспокоят, может быть рекомендовано лечение. Лечение подбирается индивидуально в зависимости от причины низкого уровня эстрогена и имеющихся симптомов.
Заместительная гормональная терапия
Обычно врачи назначают заместительную гормональную терапию (ЗГТ) при низком уровне эстрогенов.
Доступны различные типы HRT. Иногда врачи предлагают комбинированную гормональную терапию, содержащую эстроген и прогестерон.
Комбинация гормонов может быть эффективной для уравновешивания уровня эстрогена у некоторых женщин, испытывающих симптомы.
Врачи обычно назначают комбинированную ЗГТ женщинам, приближающимся к менопаузе или испытывающим постменопаузальные симптомы. Побочные эффекты от ЗГТ могут включать вздутие живота, головные боли и вагинальное кровотечение.
Женщины могут принимать ЗГТ перорально, местно, вагинально или вводить гранулы под кожу.В некоторых случаях женщинам делают укол. Приведенная доза варьируется в зависимости от человека. Обычно врачи назначают самую низкую дозу, снимающую симптомы.
Не все женщины могут использовать ЗГТ. Например, ЗГТ может не подходить для женщин, у которых в анамнезе был инсульт, сердечный приступ или высокое кровяное давление. Очень важно, чтобы любая женщина, рассматривающая ЗГТ, говорила со своим врачом о рисках, а не о пользе.
Терапия эстрогенами
Иногда врачи назначают только эстроген для лечения некоторых женщин с дефицитом эстрогена; например, женщины, которым удалили яичники.Иногда врач назначает терапию эстрогенами для лечения надоедливых симптомов менопаузы.
Похоже, что существует не так много научно доказанных методов повышения уровня эстрогена с помощью натуральных средств. Однако некоторые изменения в образе жизни и диете могут помочь.
Поддержание здорового веса
Поскольку очень низкий вес может вызвать снижение уровня эстрогена, поддержание здорового веса может помочь.
Снижение физических нагрузок
Чрезмерное количество упражнений также может вызвать снижение выработки эстрогена; поэтому сокращение упражнений может помочь повысить уровень эстрогена.
Соя
Было проведено несколько исследований о пользе сои для лечения симптомов низкого эстрогена. Существуют противоречивые исследования о пользе сои для повышения уровня эстрогена. Однако это небольшое исследование показало, что изофлавоны сои могут уменьшить симптомы менопаузы, вызванные снижением уровня эстрогена.
Увеличение количества сои может не подходить для всех женщин. Прежде чем добавлять сою или принимать соевую добавку, женщина должна поговорить со своим врачом.
Низкий уровень эстрогена может вызвать множество проблем со здоровьем и повлиять на общее самочувствие женщины.Любая женщина, у которой наблюдаются симптомы низкого эстрогена, должна поговорить со своим врачом.
Во многих случаях лечение симптомов низкого эстрогена дает хороший эффект. Хотя прогнозы различаются в зависимости от причины, часто бывает полезна ЗГТ.
Также важно помнить, что продолжительность приема ЗГТ зависит от ее ситуации.
Вы и ваши гормоны от Общества эндокринологов
Альтернативные названия эстрадиола
E2; эстрадиол; 17-бета (о) эстрадиол
Что такое эстрадиол?
Эстрадиол — стероидный гормон, вырабатываемый из холестерина, и самый сильный из трех естественных эстрогенов.Это основной эстроген, обнаруживаемый у женщин, и он выполняет множество функций, хотя в основном он действует на созревание и поддержание женской репродуктивной системы. Естественное увеличение концентрации эстрадиола в крови во время менструального цикла вызывает созревание и высвобождение яйцеклетки; то есть овулировать. Еще одна важная роль эстрадиола — утолщение слизистой оболочки матки, чтобы яйцеклетка могла имплантироваться, если она оплодотворяется. Эстрадиол также способствует развитию ткани груди и увеличивает плотность костей и хрящей.
У женщин в пременопаузе эстрадиол вырабатывается в основном яичниками. Уровни эстрадиола варьируются в течение месячного менструального цикла, самые высокие во время овуляции и самые низкие во время менструации. Уровень эстрадиола у женщин медленно снижается с возрастом, причем значительное снижение происходит в период менопаузы, когда яичники «выключаются». У беременных женщин плацента также производит много эстрадиола, особенно в конце беременности.
Мужчины также производят эстрадиол; однако производимые количества намного ниже, чем у женщин.В семенниках часть тестостерона превращается в эстрадиол, и этот эстрадиол необходим для производства спермы. У обоих полов эстрадиол в гораздо меньших количествах вырабатывается жировой тканью, мозгом и стенками кровеносных сосудов.
Как контролируется эстрадиол?
Производство эстрадиола в яичниках женщины контролируется гормонами, выделяемыми как гипоталамусом в головном мозге, так и гипофизом: это называется репродуктивной осью у женщин и также известна как ось гипоталамус-гипофиз-яичники (или гонадная).Гипоталамус в основании головного мозга выделяет гормон, называемый гонадотропин-рилизинг-гормоном. Затем гонадотропин-рилизинг-гормон воздействует на гипофиз, вызывая высвобождение еще двух гормонов, лютеинизирующего гормона (ЛГ) и фолликулостимулирующего гормона (ФСГ). ЛГ и ФСГ попадают в кровь и стимулируют яичники; в частности, ЛГ и ФСГ действуют на клетки, окружающие каждую яйцеклетку (эти клетки вместе с яйцеклеткой образуют единицу, называемую фолликулом), стимулируя рост и развитие фолликула. На последних стадиях роста и развития клетки, окружающие яйцо, вырабатывают эстрадиол.После овуляции яйцеклетки овулировавший фолликул станет желтым телом. Желтое тело вырабатывает как прогестерон, так и эстрадиол, и основная роль этих двух гормонов заключается в обеспечении полной подготовки слизистой оболочки матки к имплантации в случае оплодотворения. Количество эстрадиола (и прогестерона) в кровотоке сообщается с гипоталамусом и гипофизом, чтобы контролировать развитие яйцеклетки, овуляцию и менструальный цикл.
Что произойдет, если у меня будет слишком много эстрадиола?
У женщин слишком много эстрадиола может иметь ряд последствий.В легких случаях избыток эстрадиола может вызвать угри, запор, потерю либидо и депрессию. Более серьезные последствия могут включать увеличение веса, женское бесплодие, инсульт, сердечный приступ и повышенный риск развития рака матки и / или груди.
У мужчин слишком много эстрадиола может также вызвать сексуальную дисфункцию, потерю мышечного тонуса, увеличение жировых отложений и развитие женских качеств, таких как ткань груди. Эстрадиол становится все более доминирующим по мере того, как мужчина стареет, и его выработка тестостерона снижается, что, по мнению ученых, может быть фактором, способствующим развитию рака простаты.
Комбинированные оральные противозачаточные таблетки (таблетки) содержат синтетические формы прогестерона и эстрадиола. Таблетка предотвращает овуляцию, что делает ее почти 100% эффективной в предотвращении беременности. Помимо предотвращения овуляции, синтетические гормоны делают слизь шейки матки более густой и, следовательно, затрудняют прохождение сперматозоидов, тем самым снижая их шансы попасть в матку и яйцеводы. Синтетический эстрадиол был добавлен для предотвращения внезапного кровотечения, которое иногда возникает при приеме таблеток, содержащих только прогестерон (мини-таблетки).
Что произойдет, если у меня будет слишком мало эстрадиола?
Эстрадиол необходим для развития костей, поэтому люди с низким содержанием эстрадиола, как правило, имеют проблемы со скелетом, такие как недостаточный рост костей и остеопороз. Девочки также будут сталкиваться с проблемами в период полового созревания, такими как задержка или неспособность грудного вскармливания, нарушенный или отсутствующий менструальный цикл и бесплодие. Эстрадиол также играет важную роль в мозге, где низкие уровни могут вызывать депрессию, усталость и перепады настроения.
Выработка эстрадиола у женщин естественным образом падает в период менопаузы и вызывает многие из ее симптомов.Первоначально они включают ночную потливость, приливы, сухость влагалища и перепады настроения, а в долгосрочной перспективе у нее более вероятно развитие остеопороза. Эстрадиол используется в заместительной гормональной терапии для облегчения этих симптомов менопаузы у женщин. Есть много признанных плюсов и минусов заместительной гормональной терапии. См. Статьи о менопаузе и «Что такое ЗГТ?» Для получения дополнительной информации.
Последнее обновление: март 2018
Действительно ли дефицит эстрогена — это проблема?
«Дефицит эстрогена» — это обычное выражение.Его часто используют для описания людей, у которых последний период менструации истек на год или более. Однако дефицит эстрогена был диагностирован у 13–14-летних, только что переживших первые месячные. Или у худощавой или напряженной студентки университета, у которой внезапно прекратились менструации. Это также может быть обнаружено у подростка, у которого в конечном итоге диагностируется синдром поликистозных яичников (СПКЯ) после стойких подростковых прыщей, нежелательных волос на лице и нерегулярных периодов. Наконец, у человека с дефицитом эстрогена могут быть нерегулярные или пропущенные менструации, как у 35-летнего возраста в перименопаузе.
Странно, не правда ли, что такому количеству людей не хватает эстрогена?
Дефицит эстрогена может быть серьезным заболеванием у цисгендерных женщин. Это связано с серьезными заболеваниями, такими как остеопороз и сердечные приступы. У подростка, у которого прекратились месячные, низкий уровень эстрогена; она теряет плотность костей и рискует получить переломы в дальнейшей жизни. Женщины, живущие с СПКЯ, также подвержены повышенному риску диабета, сердечных приступов, рака эндометрия и яичников, а также бесплодия. У типичной женщины в перименопаузе повышается уровень холестерина, и у нее может быть повышенный риск сердечных приступов.Сама менопауза связана с повышенным риском остеопороза и сердечных приступов, а также с сухостью влагалища и снижением интереса к сексу.
Большая проблема с дефицитом эстрогена как симптомом или диагнозом заключается в том, что это общий термин, который играет в культурном представлении о том, что эстроген — это то, что делает женщину женщиной. Мне сейчас 77 лет, и у меня уже 20 лет менопаузы. Тем не менее, я решительно утверждаю, что у меня , а не «дефицит эстрогена». Почему? Потому что у меня низкий уровень эстрогена и прогестерона нормальный для моего возраста.А менопауза — это нормальный жизненный этап.
Существует ли вообще «дефицит эстрогена»?
Не один, это не так. Почему? Потому что сначала всегда возникает низкий уровень прогестерона (так называемый «дефицит прогестерона»). У нашего мозга есть защитная, точно настроенная реакция на многие стрессоры, поэтому нарушения овуляции, которые имеют более низкий или отсутствующий уровень прогестерона и происходят без нашего ведома в рамках регулярных циклов, происходят задолго до того, как уровень эстрогена станет низким. Кроме того, чтобы вообще вырабатывать прогестерон, в организме должен быть эстроген.Пик эстрогена в середине менструального цикла должен наступить до того, как яичники смогут выпустить яйцеклетку, а затем выработать высокий уровень прогестерона. Итак, выделение эстрогена не имеет смысла.
Вместе эстроген и прогестерон являются важной частью женской репродуктивной системы человека. Эстрадиол (разновидность эстрогена) и прогестерон действуют согласованно во время менструального цикла и взаимодействуют в обеспечении здоровой основной клеточной функции. Эстроген — важный стимулятор роста. Но рост клеток, также называемый пролиферацией, может вызвать генетические ошибки и привести к раку.Следовательно, «работа» прогестерона заключается в уменьшении эффектов пролиферации эстрогенов, а также в увеличении созревания и специализации клеток .
При описании подростка без менструации или с необычно длинными интервалами цикла (более 5 недель) единственный способ придать «дефициту эстрогена» хоть какой-то смысл — это поверить в то, что эстроген является единственным гормоном менструального цикла. Важная новая информация гласит, что для того, чтобы быть здоровой и плодородной, женщинам необходимо сбалансированное действие как эстрогена, так и прогестерона в период менструации.Это означает, что у женщин обычно есть регулярные, обычно с интервалом в месяц, овуляторные (по крайней мере, 10 дней с высоким содержанием прогестерона) менструальные циклы. Без этих сбалансированных уровней эстрогена и прогестерона в течение большей части наших менструальных лет мы подвержены риску остеопороза, сердечных приступов и рака груди и эндометрия в пожилом возрасте.
Таким образом, термин «дефицит эстрогена» не дает точного и научного описания аменореи, олигоменореи, СПКЯ, перименопаузы или менопаузы. Кроме того, он не говорит нам, какая терапия лучше всего подходит для каждой из этих потенциальных проблем на протяжении жизненного цикла женщины.Целью этих методов лечения молодых женщин должно быть восстановление здорового баланса эстроген-прогестерон с помощью регулярных овуляторных циклов.
Итак, почему мы все время слышим о «дефиците эстрогена»? Потому что это очень эффективный маркетинговый термин . Он был произведен компаниями по продаже эстрогенов и для них. Это означает, что эстроген, и только эстроген, является необходимым и эффективным лечением. Обратите внимание, что он возник в ту же эпоху, что и столь же неточный термин «заместительная гормональная терапия» или «ЗГТ».”
Таким образом, всякий раз, когда у молодой женщины пропускаются месячные (если она не беременна!), Ей не хватает и эстрогена, и прогестерона. Женщина с СПКЯ без кровотока в течение нескольких месяцев, как ни парадоксально, имеет нормальных или высокий уровень эстрогена и тестостерона, но, вероятно, низкий уровень прогестерона . Когда у женщины в перименопаузе начинается ночная потливость и предменструальные симптомы, у нее уже более высокий, чем обычно, менструальный цикл уровня эстрогена и более низкий уровень прогестерона.И когда у женщины в период менопаузы не было менструаций в течение года, ее уровень прогестерона надежно низкий, но у нее все еще может быть периодически нормальный (или даже высокий) уровень эстрогена.
Мы знаем, что у одной или двух из каждых 10 женщин старше 40 лет, у которых не было менструации в течение года, будет другой, естественный период. Женщина может сказать, что это нормальное, но «беспорядочное течение», а не рак, если у нее были болезненность груди, вздутие живота или симптомы, похожие на ПМС, до того, как это началось.
Теперь я понимаю «дефицит эстрогена».Это миф, скрывающий важность сбалансированного эстрогена и прогестерона.
Эстрогены | Лабораторные тесты онлайн
Источники, использованные в текущем обзоре
White, C. et. al. (Обновлено 17 июля 2017 г.). Анализ крови на эстрадиол. Медицинская энциклопедия MedlinePlus. Доступно в Интернете по адресу https://medlineplus.gov/ency/article/003711.htm. Доступно 07.07.18.
Беляк, К. и Харрис, Г. (27 июня 2017 г., обновлено). Аменорея. Медицинский центр акушерства и гинекологии.Доступно на сайте https://emedicine.medscape.com/article/252928-overview. Доступно 07.07.18.
Genzen, J. et. al. (Июнь 2018 г., обновлено). Аменорея. ARUP Consult. Доступно на сайте https://arupconsult.com/content/amenorrhea. Доступно 07.07.18.
(© 1995–2018). Эстрогены, эстрон (E1) и эстрадиол (E2), фракционированные, сыворотка. Клиника Мэйо Медицинские лаборатории Мэйо. Доступно на сайте https://www.mayomedicallaboratories.com/test-catalog/Clinical+and+Interpretive/84230.Доступно 07.07.18.
(ноябрь 2014 г.). Что такое эстроген? Сеть гормонального здоровья. Доступно на сайте https://www.hormone.org/hormones-and-health/hormones/estrogen. Доступно 07.07.18.
Кнудсон Дж. И Маклафлин Дж. (Август 2016 г., обновлено). Женская репродуктивная эндокринология. Руководство Merck Professional Version. Доступно на сайте https://www.merckmanuals.com/professional/gynecology-and-obstetrics/female-reproductive-endocrinology/female-reproductive-endocrinology. Доступно 07.07.18.
Софронеску А. (обновлено 18 марта 2015 г.). Эстрадиол. Медицинская лаборатория медицины. Доступно на сайте https://emedicine.medscape.com/article/2089003-overview. Доступно 07.07.18.
Источники, использованные в предыдущих обзорах
ACOG. (Октябрь 2001, номер 31). Бюллетень практики ACOG, Руководство по клиническому ведению акушеров-гинекологов, Оценка факторов риска преждевременных родов. Американский колледж акушеров и гинекологов [Руководство от Obstet Gynecol 2001: 98: 709-716].Доступно в Интернете по адресу http://www.acog.org.
MedlinePlus (3 октября 2001 г.). Медицинская энциклопедия: передозировка эстрогеном. Национальная медицинская библиотека США, Bethesda, MD. MedlinePlus. Доступно в Интернете по адресу http://www.nlm.nih.gov/medlineplus/ency/article/002584.htm.
MedlinePlus (9 августа 2001 г.). Медицинская энциклопедия: Эстрадиол — Тест. Национальная медицинская библиотека США, Bethesda, MD. MedlinePlus. Доступно в Интернете по адресу http://www.nlm.nih.gov/medlineplus/ency/article/003711.htm.
Томас, Клейтон Л., Редактор (1997). Циклопедический медицинский словарь Табера. Компания F.A. Davis, Филадельфия, Пенсильвания [18-е издание].
Пагана, Кэтлин Д. и Пагана, Тимоти Дж. (1999). Справочник по диагностическим и лабораторным испытаниям Мосби, 4-е издание: Mosby, Inc., Сент-Луис, Миссури.
Отчет с хорошей связью: Менопауза, потеря эстрогена и их лечение (март 2001 г.). На какие другие заболевания влияет эстроген? WebMDHealth, [Он-лайн сериал]. Доступно в Интернете по адресу http://my.webmd.com/content/article/1680.52622.
ACOG (3 октября 2001 г.). Исследования гормональной контрацепции изучают более простые методы регулирования менструального цикла. Американский колледж акушеров и гинекологов [Пресс-релиз]. Доступно в Интернете по адресу http://www.acog.org/from_home/publications/press_releases/nr10-31-01-3.htm.
ACOG (31 марта 2001 г.). ФЗТ и выжившие после рака эндометрия. Американский колледж акушеров и гинекологов [Пресс-релиз]. Доступно в Интернете по адресу http://www.acog.org/from_home/publications/press_releases/nr03-31-01-3.htm.
AMWA (2000). Заместительная гормональная терапия и риск рака груди, вопросы и ответы. Американская ассоциация женщин-медиков [Он-лайн сериал]. Доступно в Интернете по адресу http://www.amwa-doc.org/healthtopics/hrt_breastcancer_qa.htm.
Информационный центр женского здоровья (июнь 2001 г.). Эффективность эстрадиола для лечения депрессивных расстройств у женщин в перименопаузе. Журнал Американской медицинской ассоциации [Резюме из Arch Gen Psychiatry . 2001; 58: 529-534].Доступно в Интернете по адресу http://www.ama-assn.org.
Выходя за рамки рака (4 октября 2001 г.). Управление симптомами менопаузы Гормональные переходы. Breastcancer.org [Электронная медицинская информация]. Доступно в Интернете по адресу http://www.breastcancer.org/bey_cope_meno_horTran.html.
Drugs & Herbs (24 марта 2000 г., медицинский осмотр в октябре 2001 г.) Тропические пластыри с эстрадиолом. LycosHealth с WebMD [он-лайн медицинская информация]. Доступно в Интернете по адресу http://webmd.lycos.com/drug_article/article/4046.1242.
Ассоциация женщин за продвижение исследований и просвещения по типичным гормональным продуктам. Доступно в Интернете по адресу http://www.project-aware.org/Managing/Hrt/HRTtoday.html.
Руководство ARUP по клиническим лабораторным испытаниям. Эстриол, сыворотка и моча. Доступно в Интернете по адресу http://www.aruplab.com/guides/clt/tests/clt_a201.htm.
Руководство ARUP по клиническим лабораторным испытаниям. Скрининг материнской сыворотки. Доступно в Интернете по адресу http://www.aruplab.com/guides/clt/tests/clt_al60.htm # 1208428.
Пагана, К. Д. и Пагана, Т. Дж. (© 2007). Справочник по диагностическим и лабораторным испытаниям Мосби, 8-е издание: Mosby, Inc., Сент-Луис, Миссури. С. 416-419.
Кларк В. и Дюфур Д. Р., редакторы (© 2006). Современная практика клинической химии: AACC Press, Вашингтон, округ Колумбия. С. 359-360.
S3 Wu, A. (© 2006). Клиническое руководство Tietz по лабораторным испытаниям, 4-е издание: Saunders Elsevier, Сент-Луис, Миссури. С. 366-369, 374-377.
(обновлено 29 сентября 2009 г.).Гормоны и менопауза. Национальный институт старения [Он-лайн информация]. Доступно в Интернете по адресу http://www.nia.nih.gov/HealthInformation/Publications/hormones.htm. По состоянию на ноябрь 2009 г.
Brzyski, R. and Jensen, J. (отредактировано в марте 2007 г.). Женская репродуктивная эндокринология, Введение. Пособие Merck для специалистов здравоохранения [Он-лайн информация]. Доступно в Интернете по адресу http://www.merck.com/mmpe/sec18/ch343/ch343a.html#CACHDFBE. По состоянию на ноябрь 2009 г.
Форвик, Л. и Сторк, С.(Обновлено 26 июля 2009 г.). Эстрадиоловый тест. Медицинская энциклопедия MedlinePlus [Он-лайн информация]. Доступно в Интернете по адресу http://www.nlm.nih.gov/medlineplus/ency/article/003711.htm. По состоянию на ноябрь 2009 г.
(© 2013). Эстроген. Гормональный доктор [Он-лайн информация]. Доступно в Интернете по адресу http://thehormonedoctor.com/hormones/estrogen/. По состоянию на апрель 2014 г.
(© 1995-2013). Эстрогены, эстрон (E1) и эстрадиол (E2), фракционированные, сыворотка. Клиника Мэйо Медицинские лаборатории Мэйо [Он-лайн информация].Доступно в Интернете по адресу http://www.mayomedicallaboratories.com/interpretive-guide/?alpha=E&unit_code=84230. По состоянию на апрель 2014 г.
Meikle, A. W. и Miller, C. (обновлено в июле 2013 г.). ARUP Consult. Аменорея [Он-лайн информация]. Доступно в Интернете по адресу http://www.arupconsult.com/Topics/Amenorrhea.html?client_ID=LTD#tabs=0. По состоянию на апрель 2014 г.
Кони, П. (Обновлено 4 октября 2013 г.). Менопауза. Справочник по Medscape [Он-лайн информация]. Доступно в Интернете по адресу [Он-лайн информация].Доступно в Интернете по адресу http://emedicine.medscape.com/article/264088-overview. По состоянию на апрель 2014 г.
Беляк, К. и Попат, В. (Обновлено 5 июня 2012 г.). Аменорея. Справочник по Medscape [Он-лайн информация]. Доступно в Интернете по адресу http://emedicine.medscape.com/article/252928-overview. По состоянию на апрель 2014 г.
(пересмотрена в мае 2013 г.). Менопауза. Сеть гормонального здоровья [Он-лайн информация]. Доступно в Интернете по адресу http://www.hormone.org/diseases-and-conditions/womens-health/menopause. По состоянию на апрель 2014 г.
Гасс, М. (отредактировано в августе 2013 г.). Менопауза. Справочник Merck по домашнему здоровью [он-лайн информация]. Доступно на сайте http://www.merckmanuals.com. По состоянию на апрель 2014 г.
Пагана, К. Д. и Пагана, Т. Дж. (© 2011). Справочник по диагностическим и лабораторным испытаниям Мосби, 10-е издание: Mosby, Inc., Сент-Луис, Миссури. С. 425-428.
Кларк, У., редактор (© 2011). Современная практика в клинической химии, 2-е издание: AACC Press, Вашингтон, округ Колумбия. С. 425-428.
10 симптомов низкого эстрогена и как это лечить
Эстроген — это основной гормон, который отличает женщин от мужчин.У мужчин он есть в небольших количествах, у женщин — в гораздо большем количестве. Чтобы оставаться здоровым и чувствовать себя хорошо, важно получать достаточное количество эстрогена. Когда у нас низкий уровень этого гормона, обычно возникает множество раздражающих симптомов. Давайте рассмотрим 10 симптомов низкого уровня эстрогена и то, что мы можем сделать, чтобы их лечить.
Что делает эстроген?
Этот гормон отвечает за многие функции организма. Он поддерживает регуляцию метаболизма, чувствительности к инсулину, метаболизма глюкозы и даже веса тела.Эстроген необходим для полового развития в период полового созревания, изменения груди во время полового созревания и беременности, метаболизма холестерина и метаболизма костей. Это также помогает слизистой оболочке матки расти по мере необходимости во время менструации и на ранних сроках беременности.
Почему мы теряем эстроген?
Весь эстроген вырабатывается яичниками. Это означает, что здоровье ваших яичников напрямую связано с производством эстрогена. Во время перименопаузы яичники вырабатывают меньше эстрогена, чем раньше.Этот упадок — естественная часть жизни. Затем, когда наступает менопауза, производство эстрогена прекращается. Однако на выработку эстрогена могут влиять и другие факторы, например:
- Болезнь почек
- Нарушение функции гипофиза
- Анорексия
- Слишком много упражнений
- Яичниковая недостаточность и кисты яичников
- Возраст
- Синдром Тернера
10 симптомов низкого эстрогена
Симптомы низкого уровня эстрогена варьируются от легких до тяжелых.Взгляните на некоторые из наиболее распространенных симптомов низкого эстрогена.
1. Болезненность груди
Боль в груди — верный признак нормального низкого уровня эстрогена. Это связано с тем, что в течение части цикла, предшествующей месячным, уровень эстрогена естественным образом снижается.
2. Усталость и проблемы со сном
Эстроген тесно связан с серотонином, а серотонин образует мелатонин. Мелатонин — это основной гормон сна. Это означает, что если вы меньше спите и чувствуете усталость, возможно, у вас низкий уровень эстрогена.
3. Нерегулярные менструальные циклы
Нерегулярные циклы также указывают на низкий уровень эстрогена. Это обычное явление во время перименопаузы.
4. Исчезающие менструальные циклы
Эстроген стимулирует менструальный цикл. Если вам не хватит, цикл может полностью исчезнуть. Это нормально во время перименопаузы и, конечно, менопаузы.
5. Перепады настроения и депрессия
Эстроген вызывает выработку серотонина. Серотонин — это химическое вещество, отвечающее за хорошее настроение.Когда эстроген низкий, серотонин тоже. Некоторые исследования показывают, насколько важен эстроген для психического здоровья.
6. Головные боли
Головные боли, особенно мигрени, могут быть результатом низкого уровня эстрогена. Это происходит потому, что эстроген воздействует на химические вещества мозга, ответственные за боль.
7. Приливы и ночная потливость
Эстроген влияет на гипоталамус, регулирующий температуру тела. Низкий уровень эстрогена вызывает приливы и ночную потливость, два раздражающих симптома менопаузы и перименопаузы.
8. Частые инфекции мочевыводящих путей
Эстроген помогает слизистой оболочке уретры выполнять свою работу. А именно, чтобы не допустить попадания вредных бактерий. Низкий уровень эстрогена может привести к истончению слизистой оболочки, что облегчит проникновение бактерий. Часто следуют инфекции мочевыводящих путей.
9. Потеря костной массы
Еще одна странная вещь, которая происходит при слишком низком уровне эстрогена, — это разрушение костей. Вашим костям нужен эстроген для поддержания прочности и плотности. Они могут быстрее сломаться при низком уровне эстрогена, потому что этот гормон работает в тандеме с кальцием, витамином D и различными минералами.
10. Атрофия влагалища
Атрофия влагалища — один из наиболее серьезных симптомов низкого эстрогена, который также довольно часто встречается. Также известный как атрофический вагинит, это медленное ухудшение состояния влагалища, которое происходит с возрастом. Это заболевание влагалища характеризуется более тонким, сухим и даже сморщенным влагалищем. Воспаление часто берет верх, и секс может стать болезненным. Вы можете испытывать атрофию влагалища, если кормите ребенка грудью, вступили в перименопаузу или менопаузу, удалили яичники, у вас ранняя менопауза и / или вы принимаете лекарства от миомы матки или эндометриоза.
В большинстве случаев это состояние возникает постепенно, в течение длительного периода времени. Вы можете не осознавать, что это происходит, пока не прошло много лет после наступления менопаузы. Если у вас есть какие-либо из следующих симптомов, скорее всего, у вас атрофия влагалища:
- Вы испытываете боль во время секса
- У тебя кровотечение после секса
- Ваше влагалище суше, чем должно быть
- Ваше влагалище зудит сильнее, чем должно быть
- Горит во влагалище при мочеиспускании
- Вы чувствуете необходимость в туалет
- Вы можете почувствовать, что ваш вагинальный канал становится короче и сужается
Как лечить низкий уровень эстрогена
Заместительная гормональная терапия
Лечение низкого уровня эстрогенов часто включает заместительную гормональную терапию.Цель состоит в том, чтобы восполнить утраченный эстроген. Лечение может принимать разные формы, и ваш акушерский врач поможет вам выбрать лучшее. Влагалищные кольца, кремы с эстрогеном, вагинальные таблетки с эстрогеном, пластыри и таблетки с эстрогеном — все это возможные формы лечения эстрогеновой терапией атрофии влагалища и низкого уровня эстрогена.
Противопоказания к терапии эстрогенами включают:
- Болезнь печени
- Рак груди
- Рак эндометрия
- Тромбы или история тромбов
- Загадочное вагинальное кровотечение
Если вы не являетесь кандидатом на терапию эстрогенами, естественные методы лечения включают использование водорастворимого лубриканта для увлажнения влагалища и снятия дискомфорта.
MonaLisa Touch
MonaLisa Touch — это малоинвазивная лазерная процедура, которая иногда используется при атрофии влагалища. Это мягкое лазерное лечение работает, потому что запускает выработку коллагена в стенках влагалища. Лазерное лечение также стимулирует кровоток и увеличивает смазку. В результате влагалище начинает лучше функционировать. Анестезия не требуется. Иногда положительные результаты достигаются уже после одного сеанса MonaLisa Touch.
Ешьте для гормонального здоровья
Здоровая диета может ускорить выздоровление, независимо от того, что вас беспокоит.Вы можете есть определенные продукты для поддержания гормонального фона. Всегда ешьте как можно больше цельных продуктов и избегайте обработанных и сладких. Органические овощи и фрукты, много воды и травяных чаев, а также волокнистые продукты, такие как яблоки, груши, ягоды, авокадо, фасоль, бобовые, орехи и семена, полезны для вашего организма.
Упражнение является ключевым
Многие исследования указывают на положительное влияние физических упражнений на метаболизм эстрогенов. Мы все должны поддерживать постоянный режим упражнений. Но если вы страдаете от низкого уровня эстрогена, это еще одна причина для увеличения частоты сердечных сокращений и повышения кровообращения!
Помните, в мире нет никого, похожего на вас.Это означает, что то, что работает для одной женщины, не всегда работает для другой. Подарите себе много любви и заботы и обратите внимание на то, что вы чувствуете. Сострадание к себе имеет большое значение, когда вы имеете дело с гормональным дисбалансом. Будьте откровенны со своим врачом и расскажите ему, как вы себя чувствуете, когда обращаетесь за лечением.
В OB / GYN Associates of Alabama мы можем помочь вам понять менопаузу, гормональный дисбаланс и диапазон доступных вариантов лечения. Свяжитесь с нами, чтобы записаться на прием сегодня.
Простите! Автор не заполнил свой профиль.
Снижение преовуляторного уровня эстрадиола в сыворотке — ценный маркер для прогнозирования преждевременной овуляции в естественном / нестимулированном цикле экстракорпорального оплодотворения | Journal of Ovarian Research
Популяция и дизайн исследования
Это ретроспективное исследование пациентов, посещавших отделение вспомогательной репродукции Девятой народной больницы Медицинской школы Шанхайского университета Цзяотун с мая 2014 года по февраль 2017 года.Критериями включения в исследование было то, что пациентка проходила свой первый цикл естественного / нестимулированного ЭКО в течение периода исследования. Критериями исключения было то, что у пациента не измеряли уровень E2 после преждевременных скачков ЛГ или триггеров ХГЧ / ГнРГ. Уменьшение резерва яичников (DOR) определялось либо по уровню сывороточного ФСГ ≥11,4 мМЕ / мл на 3-й день, либо по общему количеству антральных фолликулов ≤4 [17].
Естественные / нестимулированные циклы
Естественные / нестимулированные циклы были выполнены, как показано в Дополнительном файле 1: Рисунок S1.Размер фолликулов и уровень ФСГ, ЛГ, Е2 и Р в сыворотке измеряли с третьего дня менструального цикла, и во время развития фолликула лекарство не применялось. Когда диаметр доминантного фолликула был ≥18 мм, уровень E2 ≥ 200 пг / мл и уровень ЛГ <20 мМЕ / мл, овуляция вызывалась с помощью трипторелина (0,1 мг; декапептил, Ferring Pharmaceuticals, Мальмо, Швеция) или ХГЧ 5000 МЕ (Lizhu Pharmaceutical Trading Co., Чжухай, Китай) в 23:00. Трансвагинальное извлечение ооцитов под контролем УЗИ проводилось через 32–34 ч после включения триггера.Уровни сывороточного ФСГ, ЛГ, E2 и P были измерены через 10 часов. Если уровень E2 у пациента снизился, забор яйцеклетки (OPU) проводился либо по расписанию, либо немедленно, в зависимости от предпочтения врача. Если уровни ЛГ были ≥ 20 мМЕ / мл (преждевременный выброс ЛГ), сывороточные уровни ФСГ, ЛГ, E2 и P измерялись днем (шесть часов спустя), а OPU проводился в 8:00 следующего утра, как запланировано. Если уровни E2 снизились, OPU выполнялся либо по расписанию, либо немедленно. Все фолликулы диаметром более 10 мм были аспирированы.Оплодотворение аспирированных ооцитов проводили in vitro с использованием либо обычного оплодотворения, либо интрацитоплазматической инъекции сперматозоидов (ИКСИ), в зависимости от параметров спермы. Эмбрионы были исследованы на количество и регулярность бластомеров и степень эмбриональной фрагментации на третий день в соответствии с критериями, описанными Cummins et al. [18]
Было большое количество естественных циклов без эмбрионов, а развивающиеся эмбрионы часто были непредсказуемыми. Более того, преждевременные скачки ЛГ и повышенный уровень фосфора могут повлиять на результат переноса эмбрионов в естественном цикле.Поэтому для всех циклов ЭКО / ИКСИ применялась стратегия «заморозить все». Все высококачественные эмбрионы, включая 8-клеточные эмбрионы степени І и степени II, были заморожены посредством витрификации на третьи сутки после извлечения ооцитов. Только некачественные эмбрионы помещали в расширенную культуру до тех пор, пока они не достигли стадии бластоцисты. Во время этой стадии замораживали только бластоцисты хорошей морфологии на 5-й или 6-й день. Процедуру витрификации для замораживания эмбрионов и бластоцист на стадии дробления выполняли, как описано ранее [19].
Для оттаивания последовательно использовали растворы 1 М, 0,5 М и 0 М сахарозы в качестве разведения криопротекторов. Все этапы стеклования и нагревания выполнялись при комнатной температуре, за исключением первого этапа нагревания, который проводился при 37 ° C. Для подготовки эндометрия было рекомендовано заместительное гормональное лечение. Вкратце, этинилэстрадиол 25 мкг Tid (Xinyi Pharmaceutical Co., Шанхай, Китай) вводили в течение 14 дней, а затем курс лечения был переведен на 4 Femoston (Abbott Healthcare Products, B.V., Weesp, Нидерланды) желтые пероральные таблетки ежедневно (8 мг эстрадиола и 40 мг дидрогестерона) и мягкие вагинальные капсулы прогестерона (Utrogestan 200 мг Bid, Laboratoires Besins-Iscovesco, Париж, Франция). Перенос эмбрионов был организован через 3 дня. Перенос бластоцисты проводили через 5 дней. После наступления беременности прием экзогенных эстрогенов и прогестерона продолжался до 10 недель беременности.
Анализ гормонов
Уровни ФСГ, ЛГ, E2 и P в сыворотке измеряли на MC3, в день триггера, день после триггера (примерно через 10 ч после инъекции ГнРГ / ХГЧ) и через шесть часов после ЛГ ≥20 мМЕ / мл.Уровни гормонов измеряли с помощью хемилюминесценции (Abbott Biologicals B.V., Weesp, Нидерланды). Используемые нижние пределы чувствительности составляли 0,06 мМЕ / мл для ФСГ, 0,09 мМЕ / мл для ЛГ, 10 пг / мл для E2 и 0,1 нг / мл для P. Верхний предел для измерения E2 был установлен на уровне 5000 пг / мл. и уровни были зарегистрированы как 5000 пг / мл, если они были выше верхнего предела в день запуска или на следующий день после запуска.
Статистический анализ
Скорость извлечения ооцитов определялась как отношение общего количества извлеченных ооцитов к количеству фолликулов диаметром ≥ 10 мм, аспирированных в день извлечения ооцитов.Степень зрелости ооцитов определяли как отношение MII-ооцитов к количеству собранных ооцитов. Живорождение было определено как рождение живого ребенка после 28 недель беременности. Клиническая беременность определялась как наличие гестационного мешка с сердечной активностью плода во время ультразвукового исследования через 7 недель после FET. Скорость имплантации определялась как количество гестационных мешков, деленное на количество перенесенных эмбрионов.
Для непрерывных переменных сравнения между группами анализировали с помощью ANOVA с последующим соответствующим апостериорным тестом или t-критерием.Для категориальных переменных использовался критерий хи-квадрат Пирсона или точный критерий Фишера для изучения различий. P -значения менее 0,05 считались статистически значимыми. Модель логистической регрессии использовалась для количественной оценки влияния связанных факторов на преждевременную овуляцию. Учитывались следующие факторы: возраст женщины, базальный уровень ФСГ, тип триггера (преждевременный выброс ЛГ или триггер ХГЧ / ГнРГ) и преовуляторное соотношение E2 / -1E2. Все факторы были введены в регрессионную модель.Данные в таблице представлены как среднее значение и 95% доверительный интервал (ДИ) среднего. Анализ рабочей кривой приемника (ROC) использовался для оценки и сравнения точности прогноза отношения (преовуляторный E2 / — 1E2). Оптимальное пороговое значение для отношения изменения E2 было определено с использованием значения, которое максимизирует меру чувствительности + специфичности — 1. Кривые ROC и все другие данные были проанализированы с использованием Статистического пакета для социальных наук для Windows (версия 22, SPSS Inc.).
Дефицит эстрогена — обзор
Эффекты дефицита эстрогена
Дефицит эстрогена приводит как к краткосрочным, так и к долгосрочным эффектам, и люди различаются по типу и тяжести встречающихся осложнений. У большинства пациентов с гипопитуитаризмом в течение длительного периода времени наблюдается дефицит гонадотропинов, но пациенты с новым началом гипоталамо-гипофизарного заболевания или хирургического вмешательства могут испытывать вазомоторную нестабильность, утомляемость, нарушение настроения и сексуальную дисфункцию различной степени.Последнее в основном связано с атрофическим изменением эпителия влагалища.
Долгосрочные последствия дефицита эстрогена часто наблюдаются у женщин с ранним началом гипопитуитаризма, которым не проводилась заместительная терапия эстрогенами. Наиболее важным последствием является снижение минерализации костей, что приводит к повышенному риску остеопоротического перелома. Развитие остеопороза у человека зависит от достигнутого пика массы костной ткани взрослого человека и последующей скорости потери костной массы. Генетические факторы являются наиболее важными детерминантами максимальной костной массы; однако дефицит эстрогена в подростковом и раннем взрослом возрасте способствует снижению минерализации костей.Таким образом, начало дефицита эстрогена как в раннем возрасте, так и в более позднем возрасте (после достижения максимальной костной массы) может повлиять на здоровье костей. МПК можно оценить с помощью различных методов, включая количественную компьютерную томографию (КТ), фотонную абсорбциометрию и двухэнергетическую рентгеновскую абсорбциометрию (ДРА). Широкая клиническая доступность и относительная дешевизна DXA означает, что эндокринологи все чаще используют этот инструмент для оценки здоровья костей и мониторинга эффекта лечения у пациентов с гипогипофизом.
Дислипидемия — другое серьезное долгосрочное последствие дефицита эстрогена. Циркулирующий эстрадиол изменяет метаболизм липопротеинов, что приводит к снижению холестерина ЛПНП и увеличению холестерина ЛПВП. Использование замещения эстрогенов благоприятно влияет на липидный профиль; однако андрогенные прогестины могут частично этому противодействовать.

 Значения эстрадиола в первой фазе низкие, отсутствует второй пик лютеиновой фазы
Значения эстрадиола в первой фазе низкие, отсутствует второй пик лютеиновой фазы
Добавить комментарий